|
|
马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
Shaji, S., R.K. Selvaraj and R. Shanmugasundaram, Salmonella Infection in Poultry: A Review on the Pathogen and Control Strategies. Microorganisms, 2023. 11(11): p. 2814.
01摘要
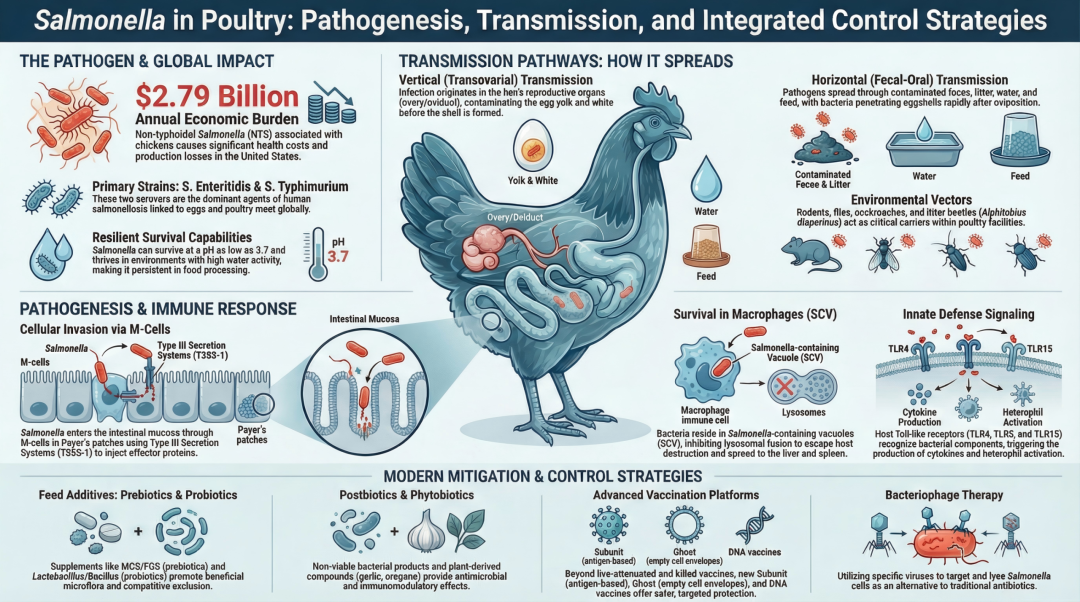
沙门氏菌(Salmonella)是全球范围内导致食源性人畜共患病的主要病原体之一。非伤寒沙门氏菌(Non-typhoidal Salmonella, NTS)血清型是与家禽沙门氏菌病相关的首要病原体。被污染的禽蛋和禽肉产品是人类感染沙门氏菌的最主要来源。在鸡群中,水平传播(环境至宿主)和垂直传播(母体至子代)是其主要的感染途径。与家禽中沙门氏菌发病机制相关的主要毒力基因位于沙门氏菌致病岛1和2(SPI-1和SPI-2)内。家禽抵御沙门氏菌入侵的防御机制涉及复杂的细胞介导免疫和体液免疫反应。目前,为了减轻家禽生产链中的沙门氏菌负荷,业界广泛采用鸡群疫苗接种以及在饲料中添加益生元、益生菌、后生元、合生元和噬菌体等饲料添加剂的策略。尽管存在多种控制措施,但家禽养殖业仍然迫切需要一种广泛、安全且机制明确的综合干预策略,以便为家禽提供抵御各种沙门氏菌血清型的长期保护。本文基于2023年最新的研究进展,对沙门氏菌的病原学特征、致病机制、宿主免疫应答以及当前和未来的防控策略进行全面、深度的综述。
02引言 (Introduction)
在现代全球化的农业与食品生产体系中,家禽业占据着举足轻重的地位,为全球人口提供了高质量、低成本的动物蛋白。然而,家禽养殖系统也成为了多种病原微生物的温床,其中最受关注的公共卫生威胁便是沙门氏菌(Salmonella)。根据世界卫生组织(WHO)和美国疾病控制与预防中心(CDC)的流行病学追踪数据,沙门氏菌是引发全球细菌性肠胃炎的首要原因。
人类主要通过摄入受污染的动物源性食品(特别是家禽肉类和未经充分加热的鸡蛋)感染非伤寒沙门氏菌。这种感染不仅给人类健康带来了巨大的负担(表现为腹泻、发烧、腹部绞痛,甚至在免疫力低下人群中引发致命的系统性菌血症),同时也给全球家禽业造成了不可估量的经济损失。这些损失包括动物死亡率的增加、生产性能(如产蛋率和饲料转化率)的下降,以及为了满足严格的食品安全标准而产生的昂贵的病原体检测和扑杀成本。
为了应对这一挑战,科学界和兽医学界进行了长达数十年的研究,以期彻底解析沙门氏菌在家禽宿主中的定植机制、传播动力学以及宿主-病原体的免疫博弈。本综述旨在系统性地梳理沙门氏菌感染家禽的最新研究成果,从病原体本身的生物学特性出发,深入探讨其复杂的致病分子机制,并全面评估当前家禽业正在采用及研发中的各类生物学与管理防控策略。
03病原学与血清型分类(Etiology and Serovars)
沙门氏菌是一种革兰氏阴性、兼性厌氧、通常具有鞭毛(可运动)的杆状细菌,属于肠杆菌科。从分类学角度来看,沙门氏菌属分为两个主要物种:肠道沙门氏菌(Salmonella enterica)和邦戈沙门氏菌(Salmonella bongori)。其中,S. enterica 包含超过2600种已知的血清型(Serovars),这些血清型是基于Kauffmann-White-Le Minor微量凝集方案,通过分析其表面抗原——体细胞(O)抗原、鞭毛(H)抗原和荚膜(Vi)抗原的多态性来划分的。
在家禽病理学和流行病学中,感染鸡群的肠道沙门氏菌血清型可以根据其宿主特异性和临床表现分为两大核心类别:宿主特异性/适应性沙门氏菌和非宿主特异性(泛宿主)沙门氏菌。
2.1 宿主特异性沙门氏菌 (Host-Specific Serovars)
此类沙门氏菌高度适应禽类宿主,很少感染人类。它们会引起家禽的严重系统性疾病,导致极高的发病率和死亡率。- 鸡白痢沙门氏菌 (S. enterica serovar Pullorum): 主要引起幼禽(特别是出壳后前几周的雏鸡)的鸡白痢(Pullorum disease)。症状包括白色糊状粪便、闭眼、呼吸困难及高死亡率。存活的个体往往成为终身带菌者。
- 鸡伤寒沙门氏菌 (S. enterica serovar Gallinarum): 引发鸡伤寒(Fowl typhoid),主要影响成年禽类,表现为极度虚弱、冠和肉垂苍白或发绀、黄绿色腹泻以及肝脾肿大,同样具有高致死性。
2.2 非宿主特异性沙门氏菌 (Non-Host-Specific Serovars)
这些血清型,通常被称为副伤寒沙门氏菌(Paratyphoid Salmonella),不仅能在禽类肠道内定植,更是引发人类食源性疾病的罪魁祸首。- 肠炎沙门氏菌 (S. Enteritidis): 目前全球范围内与鸡蛋污染最密切相关的血清型。它具有独特的亲生殖道特性,能定植在母鸡的卵巢和输卵管中,在鸡蛋形成内部时便造成污染。
- 鼠伤寒沙门氏菌 (S. Typhimurium): 广泛存在于多种动物宿主中,通常通过家禽肉类加工过程中的交叉污染传播给人类。
- 其他新兴血清型: 如海德堡沙门氏菌(S. Heidelberg)、婴儿沙门氏菌(S. Infantis)和肯塔基沙门氏菌(S. Kentucky),近年来在家禽群中的检出率呈上升趋势。
表1:影响家禽的主要沙门氏菌血清型及其致病特征总结[td]| 沙门氏菌血清型 (Serovar) | 宿主范围 | 家禽临床疾病 | 人类致病性 (公共卫生意义) | 主要传播媒介 | | S. Pullorum (鸡白痢沙门氏菌) | 高度禽类特异性 | 鸡白痢 (幼禽高死亡率,白色腹泻) | 极低 | 垂直传播、水平接触 | | S. Gallinarum (鸡伤寒沙门氏菌) | 高度禽类特异性 | 鸡伤寒 (成年禽系统性感染) | 极低 | 垂直传播、环境污染 | | S. Enteritidis (肠炎沙门氏菌) | 广泛 (多宿主) | 副伤寒感染 (通常为亚临床/无症状定植) | 极高 (引发人类胃肠炎) | 受污染的鸡蛋 (内部) 和禽肉 | | S. Typhimurium (鼠伤寒沙门氏菌) | 广泛 (多宿主) | 副伤寒感染 (多数亚临床,幼禽可致病) | 极高 (引发人类胃肠炎) | 受污染的禽肉产品、环境交叉污染 | | S. Heidelberg / S. Infantis | 广泛 (多宿主) | 无症状肠道定植 | 高 (部分菌株具有多重耐药性) | 加工过程中的胴体污染 |
04沙门氏菌在家禽中的传播途径 (Transmission Routes)
沙门氏菌在现代高度集约化的家禽生产链中的传播呈现出复杂的多维动态过程。要有效控制该病原体,必须深入理解其水平和垂直两大传播途径。
3.1 水平传播 (Horizontal Transmission)
水平传播是沙门氏菌在同一世代家禽群体内扩散的最常见方式。它涉及病原体从受感染个体向易感个体的直接或间接转移。- 粪口途径 (Fecal-Oral Route): 受感染的家禽通过粪便排出大量沙门氏菌。健康鸡只通过啄食受污染的垫料、粪便或含有病菌的尘埃颗粒而感染。
- 饲料和水源污染: 动物源性饲料原料(如肉骨粉、鱼粉)是历史上的主要污染源。水线如果不进行定期消毒,容易形成含有沙门氏菌的生物被膜(Biofilms),成为持续的感染源。
- 媒介生物 (Vectors): 昆虫(如黑甲虫 Alphitobius diaperinus、苍蝇)、啮齿动物(老鼠)以及野生鸟类可以在农场内外携带和机械传播沙门氏菌。
- 生物安全漏洞: 工作人员的靴子、衣物、农场设备及运输车辆未能严格消毒,也是导致农场间交叉感染的重要原因。
3.2 垂直传播 (Vertical Transmission)
垂直传播,又称经卵传播(Transovarian transmission),是肠炎沙门氏菌(S. Enteritidis)和鸡白痢/鸡伤寒沙门氏菌极为高效的隐蔽传播策略。- 直接内部污染: 沙门氏菌从肠道逃逸后,通过菌血症途径到达生殖器官。它们能够侵入并定植于母鸡的卵巢和输卵管(特别是峡部和膨大部)。在卵黄形成或蛋清分泌的过程中,细菌被直接包裹在鸡蛋内部。这种被包裹在蛋壳内部的病原体对表面消毒剂具有完全的抵抗力。
- 间接外部污染: 鸡蛋在产出通过泄殖腔时,或产出后落在受污染的垫料上,蛋壳表面被沙门氏菌污染。随着温度变化产生的压差,沙门氏菌可通过蛋壳上的微孔穿透进入蛋内。
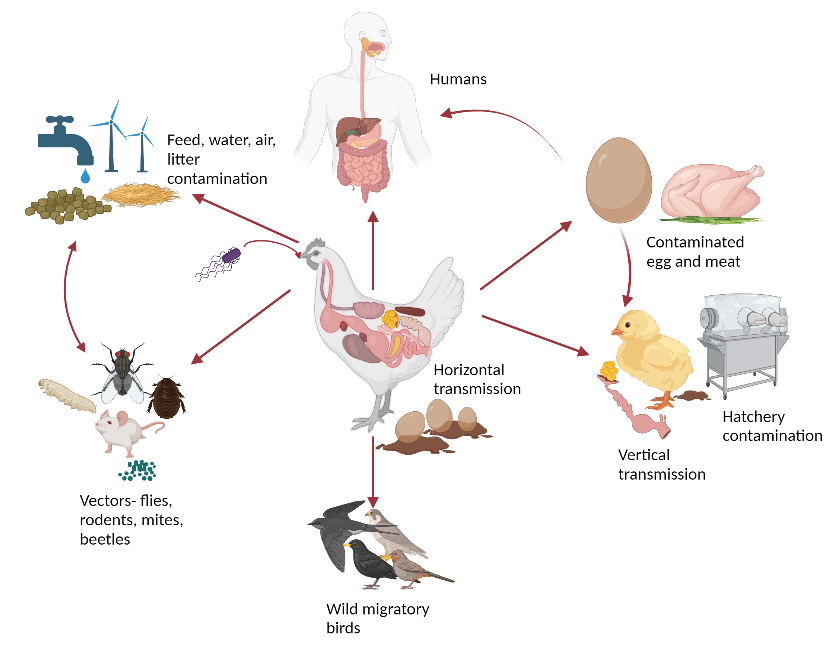
图 1. 沙门氏菌在家禽生产系统中的传播动力学。该图展示了沙门氏菌通过垂直途径(被感染母鸡的生殖道将病原体传递至鸡蛋内部,随后孵化出带菌雏鸡)和水平途径(通过受污染的饲料、水、垫料、啮齿动物和农场工作人员在鸡群间传播)的循环过程。
04致病机制与毒力因子 (Pathogenesis and Virulence Factors)
非伤寒沙门氏菌在家禽体内建立感染并长期定植,依赖于一套高度精密的基因调控网络和结构复杂的毒力装置。其致病过程大致可分为:肠道吸附、上皮细胞入侵、巨噬细胞内存活及系统性播散。
4.1 肠道定植与吸附
当沙门氏菌经口进入家禽消化道后,它们必须克服胃酸和肠道胆盐的恶劣环境。到达盲肠和回肠后,细菌利用表面的纤毛(Fimbriae,特别是I型纤毛)、鞭毛和非菌毛黏附素,与家禽肠道上皮细胞的微绒毛表面的受体牢固结合,从而抵抗肠蠕动带来的机械清除。
4.2 沙门氏菌致病岛 (Salmonella Pathogenicity Islands, SPIs)
沙门氏菌基因组中存在多个获得性基因簇,称为致病岛,它们是沙门氏菌从非致病性共生菌进化为兼性胞内病原体的关键标志。其中,SPI-1和SPI-2的作用最为核心,它们分别编码了各自独立的三型分泌系统(Type III Secretion Systems, T3SS)。
4.2.1 SPI-1 与 T3SS-1:介导细胞入侵
SPI-1主要在细菌感染的早期阶段发挥作用,其编码的T3SS-1形成了一种类似“分子注射器”的跨膜结构复合物。- 机制: 当沙门氏菌接触到宿主肠道上皮细胞(包括M细胞和吸收性肠上皮细胞)时,T3SS-1组装完成,将一系列效应蛋白(Effector proteins,如SipA, SipC, SopB, SopE, SopE2)直接注入宿主细胞的细胞质中。
- 效应: 这些效应蛋白具有激酶或鸟苷酸交换因子(GEF)活性,它们挟持宿主细胞的肌动蛋白细胞骨架(Actin cytoskeleton)网络,通过激活Rho家族的GTP酶(如Cdc42和Rac1),引起宿主细胞膜发生剧烈的形变,形成“膜皱褶”(Membrane ruffling)。这种由细菌主动诱发的巨胞饮(Macropinocytosis)作用,迫使非吞噬性的肠上皮细胞将沙门氏菌吞入胞内,形成沙门氏菌包裹液泡(SCV)。
4.2.2 SPI-2 与 T3SS-2:介导胞内生存
成功进入宿主细胞内部后,沙门氏菌面临的下一个挑战是避免被溶酶体降解。此时,细菌感知到胞内SCV的微环境(低pH值、低钙、缺乏营养),从而下调SPI-1的表达,并激活SPI-2。- 机制: SPI-2编码的T3SS-2开始在SCV膜上组装,并将第二波效应蛋白(如SifA, SseF, SseG, SteC等)注入宿主细胞质。
- 效应: T3SS-2的效应蛋白协同作用,不仅阻止了SCV与破坏性的溶酶体融合,还通过招募微管和高尔基体来源的囊泡,重塑SCV的膜结构,形成沙门氏菌诱导细丝(Salmonella-induced filaments, Sifs)。这为细菌提供了一个安全的内体复制生态位(Replicative niche),使其能够在巨噬细胞等免疫细胞内部存活、增殖,并随着巨噬细胞的游走,将其播散到肝脏、脾脏、卵巢等全身器官,形成隐性全身感染。
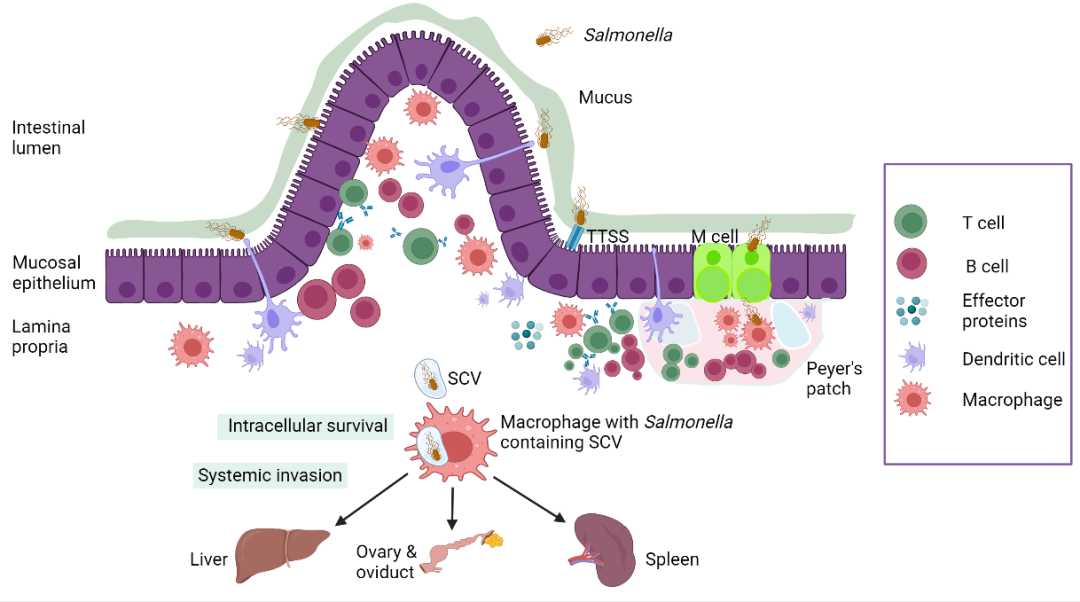
图 2. 沙门氏菌致病岛介导的分子致病机制。图解显示了SPI-1编码的T3SS-1注射SopE/SopB等效应蛋白诱导肠上皮细胞膜皱褶的侵入过程,以及沙门氏菌被吞噬后,通过SPI-2编码的T3SS-2阻止吞噬体-溶酶体融合,并在沙门氏菌包裹液泡(SCV)中存活和增殖的分子级联反应。
05宿主免疫反应 (Host Immune Response)
家禽免疫系统在与沙门氏菌的进化博弈中,发展出了一套精密的防御机制。免疫反应可分为先天性(快速但不具有特异性)和适应性(相对缓慢但具有高度特异性和记忆性)两大部分。
5.1 先天性免疫反应 (Innate Immunity)
先天免疫是家禽抵抗沙门氏菌的第一道防线。肠道上皮细胞和驻留的吞噬细胞(如巨噬细胞、异嗜性白细胞)通过其表面或胞内的模式识别受体(Pattern Recognition Receptors, PRRs)来检测病原体相关分子模式(PAMPs)。
5.1.1 禽类Toll样受体 (Toll-like Receptors, TLRs)
在鸟类中,TLRs的表达具有一定的特异性(如缺乏哺乳动物的TLR9,而以TLR21行使类似功能;拥有鸟类特有的TLR15)。- 当沙门氏菌侵入时,其细胞壁组分如脂多糖(LPS)被TLR4识别。
- 沙门氏菌的CpG未甲基化DNA片段被TLR21识别。
- 鸟类特有的TLR15能够识别沙门氏菌分泌的蛋白酶并引发强烈的炎症信号。
表2:禽类Toll样受体(TLRs)及其在沙门氏菌感染中的配体识别机制| 禽类受体类型 | 靶向病原体相关分子模式 (PAMP) | 沙门氏菌对应配体 | 细胞定位 | 下游信号通路与主要功能 | | TLR2 | 肽聚糖 (Peptidoglycan), 脂蛋白 | 细菌细胞壁成分 | 细胞膜表面 | MyD88依赖性通路,刺激前炎症细胞因子分泌 | | TLR4 | 脂多糖 (Lipopolysaccharide, LPS) | 革兰氏阴性菌LPS (内毒素) | 细胞膜表面 | MyD88及TRIF通路,核心炎症反应激活器 | | TLR5 | 鞭毛蛋白 (Flagellin) | 沙门氏菌鞭毛抗原 (H抗原) | 细胞膜表面 | 强效诱导趋化因子,招募异嗜性白细胞 | | TLR15 | 蛋白酶 (Proteases) | 沙门氏菌来源的特定外切酶 | 细胞膜/内体 | 鸟类特有,激活促炎因子介导抗菌反应 | | TLR21 | 含有未甲基化CpG基序的DNA | 沙门氏菌基因组DNA | 内体 (Endosome) 膜 | 功能同哺乳动物TLR9,诱发强烈的Th1型应答 |
未完待续......
来源:菌中无戏言
|
|