|
|
马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
接上篇:【分享】家禽中的沙门氏菌感染:病原体及防控策略(上)
5.1.2 炎症介质与细胞招募
TLRs被激活后,通过MyD88等接头蛋白启动NF-κB信号通路,导致促炎细胞因子(如IL-1β, IL-6, IL-18)和趋化因子(如CXCLi1, CXCLi2)的大量转录和释放。趋化因子迅速将大量的异嗜性白细胞(Heterophils,家禽中相当于哺乳动物的中性粒细胞)和巨噬细胞招募至肠道感染部位。异嗜性白细胞通过脱颗粒作用释放抗菌肽、溶菌酶和活性氧(ROS)来直接杀灭细胞外的沙门氏菌。
5.2 适应性免疫反应 (Adaptive Immunity)
随着感染的持续,先天免疫细胞(主要是树突状细胞和巨噬细胞)作为抗原递呈细胞(APCs),将沙门氏菌抗原加工后通过MHC-I或MHC-II分子展示给T淋巴细胞,从而启动适应性免疫。
5.2.1 细胞介导免疫 (Cell-Mediated Immunity, CMI)
针对兼性胞内寄生的沙门氏菌,强大的细胞介导免疫是清除感染(特别是系统性肝脾感染)的绝对关键。- CD4+ T 辅助细胞 (Th1型): 被抗原激活的CD4+ T细胞大量分化为Th1亚型,并分泌大量的干扰素-γ (IFN-γ)。IFN-γ是巨噬细胞的强效激活剂。它促使被感染的巨噬细胞上调一氧化氮合成酶(iNOS)的表达,产生大量的一氧化氮(NO),打破沙门氏菌T3SS-2构建的安全防线,彻底杀死寄生在吞噬体内的沙门氏菌。
- CD8+ 细胞毒性T细胞 (CTLs): 负责识别并直接裂解那些被沙门氏菌深度感染且无法通过自身机制清除病菌的宿主细胞,切断病菌的复制源。
5.2.2 体液免疫 (Humoral Immunity)
B淋巴细胞在Th2细胞的辅助下成熟并分化为浆细胞,产生针对沙门氏菌O抗原和H抗原的特异性抗体。- IgY (家禽的IgG等效物): 主要在血液中循环,通过调理吞噬作用(Opsonization)增强巨噬细胞对游离沙门氏菌的捕获,并能激活补体经典途径。
- IgA: 主要分泌在肠道粘膜表面。分泌型IgA(sIgA)能在沙门氏菌接触肠上皮细胞前将其凝集,阻止其吸附和定植(免疫排斥)。
- 母源抗体转移: 种鸡血液中的特异性IgY可以通过卵黄转移给雏鸡,IgA和IgM则转移到蛋清中,为初生雏鸡提供早期被动免疫保护。
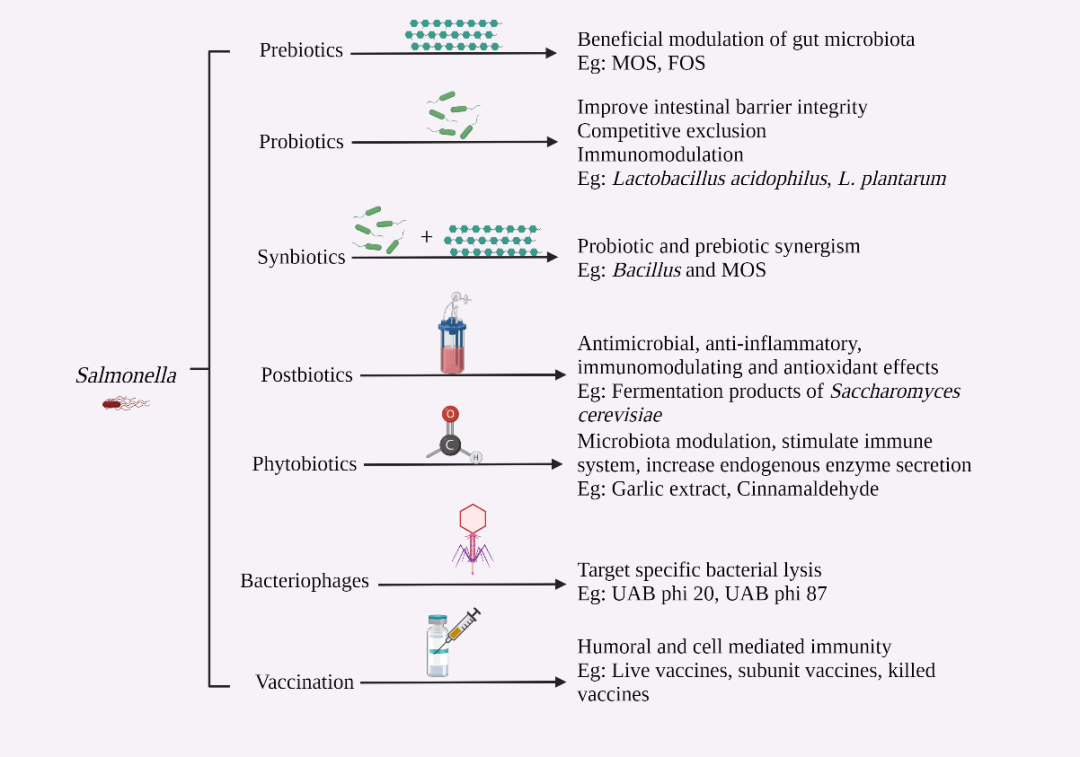
图 3. 家禽肠道免疫系统针对沙门氏菌的综合免疫应答全景图。图中展示了异嗜性白细胞的招募(先天免疫)、巨噬细胞的抗原递呈、CD4+ T细胞释放IFN-γ激活杀菌机制(细胞免疫),以及B细胞分泌IgA/IgY进行抗体中和(体液免疫)的协同过程。
06家禽沙门氏菌的现代防控策略 (Control Strategies)
鉴于沙门氏菌能够在禽舍环境中顽强存活并具有多途径传播的能力,单一的控制手段往往注定失败。目前,家禽产业正在实施涵盖从“农场到餐桌”全产业链的多维干预策略。
6.1 疫苗接种 (Vaccination)
疫苗接种是预防蛋鸡和种鸡沙门氏菌感染的基石,目的是减少肠道定植、防止生殖道入侵,并减少垂直传播。目前的疫苗类型主要有以下几种:
- 减毒活疫苗 (Live Attenuated Vaccines):
○ 原理与优势: 通过化学诱变或基因工程手段敲除沙门氏菌的致病基因(如芳香族氨基酸合成基因aroA、或者代谢调控基因cya/crp双缺失突变体)。活疫苗能够模拟自然感染,同时引发强烈的细胞免疫(CMI)、粘膜免疫(IgA)和体液免疫。对于清除胞内沙门氏菌,这被认为是目前最有效的疫苗类型。○ 局限性: 存在毒力返祖的潜在风险;可能与农场的沙门氏菌野外监测程序产生交叉反应;对日龄极小的雏鸡可能具有微弱的致病性。 - 灭活疫苗 / 菌苗 (Inactivated Vaccines / Bacterins):
○ 原理与优势: 含有被福尔马林或热杀死的沙门氏菌全菌体,通常与油乳剂等佐剂结合使用。绝对安全,不存在毒力返祖的风险。它们能诱导产生极高滴度的循环抗体(IgY),在预防母鸡向鸡蛋内部的垂直转移方面效果显著。○ 局限性: 几乎不诱发细胞免疫,且无法刺激肠道产生局部粘膜免疫(IgA),因此在防止肠道定植方面的效力不如活疫苗。通常需要多次注射,增加劳动成本。 - 重组与亚单位疫苗 (Recombinant and Subunit Vaccines):
○ 原理: 仅使用沙门氏菌的特定抗原成分(如外膜蛋白OMPs、鞭毛蛋白FliC)。安全性极高,且易于通过基因工程进行大规模生产。当前研究热点是利用无害载体(如减毒的大肠杆菌或乳酸菌)表达沙门氏菌抗原。 - DNA疫苗 (DNA Vaccines):
○ 前沿方向: 将编码沙门氏菌保护性抗原的质粒DNA直接注入家禽体内,利用宿主细胞表达抗原并提呈给免疫系统。目前在禽病学中仍处于实验室开发阶段,面临投递效率(Delivery efficiency)等挑战。
表3:家禽沙门氏菌疫苗类型及其免疫学特性比较| 疫苗类型 | 主要代表性成分/突变株 | 免疫激活类型 | 主要优势 | 主要劣势/局限性 | | 减毒活疫苗 | aroA突变株, cya/crp突变株 | 强烈的细胞免疫(CMI)、粘膜免疫、体液免疫 | 效果全面,模拟自然感染,可快速提供交叉保护 | 潜在的毒力返祖风险,可能干扰血清学监测 | | 灭活疫苗(菌苗) | 福尔马林灭活全菌 + 佐剂 | 主要为强大的体液免疫(循环IgY) | 绝对安全,极大降低垂直传播率和鸡蛋污染 | 几乎无细胞免疫和肠道局部免疫,需注射操作 | | 重组亚单位疫苗 | 纯化的鞭毛蛋白(FliC), 外膜蛋白(OMPs) | 体液免疫为主,可通过佐剂调节 | 安全性极高,靶点明确,适合标记疫苗开发 | 免疫原性可能相对较弱,需要高效的新型佐剂 | | DNA疫苗 | 携带毒力基因序列的质粒(如构建的针对SPI-1蛋白的核酸片段) | 细胞免疫与体液免疫并重 | 研发速度快,无感染风险,易于构建多价疫苗 | 在家禽中的递送技术尚不成熟,成本较高 |
6.2 饲料添加剂与抗生素替代品 (Feed Additives and Alternatives to Antibiotics)
全球对农畜产业中预防性抗生素使用(AGPs)的禁令正在加速,这催生了大量致力于调节肠道微生物群和增强肠道屏障功能的抗生素替代品的应用。
6.2.1 益生菌 (Probiotics)
益生菌是活的微生物制剂,当摄入足够数量时能为宿主带来健康益处。在家禽中,常用的益生菌包括乳酸杆菌(Lactobacillus spp.)、双歧杆菌(Bifidobacterium spp.)、肠球菌(Enterococcus)和枯草芽孢杆菌(Bacillus subtilis)。- 机制 - 竞争性排斥 (Competitive Exclusion, CE): 基于经典的“Nurmi概念”,益生菌在肠道黏膜上占据生态位(受体结合位点),物理性地阻挡沙门氏菌的附着。
- 机制 - 抗菌物质产生: 乳酸菌通过发酵产生乳酸、乙酸等,降低肠道pH值至沙门氏菌无法耐受的程度。此外,它们还能分泌细菌素(Bacteriocins)和过氧化氢,直接抑制致病菌的生长。
6.2.2 益生元 (Prebiotics)
益生元是不可消化的碳水化合物(如低聚果糖FOS、甘露寡糖MOS、半乳寡糖GOS),它们能够选择性地刺激肠道内有益菌群的生长和活性。- 机制: 有益菌发酵益生元产生大量的短链脂肪酸(SCFAs),如丁酸(Butyrate)。丁酸不仅能显著降低肠道微环境pH值,更重要的是,它是肠上皮细胞首选的能量来源,能够促进绒毛生长,增强肠道紧密连接(Tight junctions),极大提升肠道上皮屏障的物理完整性。此外,某些寡糖(如MOS)具有类似病原体受体的结构,能够像“诱饵”一样结合沙门氏菌的1型纤毛,使其随粪便排出而无法定植。
6.2.3 合生元 (Synbiotics) 与 后生元 (Postbiotics)
- 合生元: 是益生菌和益生元的混合物。其设计理念是利用益生元为特定益生菌提供专属“干粮”,从而提高益生菌在肠道内的存活率和植入成功率,发挥“1+1>2”的协同抗菌效应。
- 后生元: 这是一个新兴概念,指益生菌的无生命代谢产物、细胞壁碎片或裂解物(如酵母细胞壁提取物、肽聚糖片段)。与活的益生菌相比,后生元具有绝对的安全性和优异的贮存稳定性,其分子能够直接被肠道免疫细胞的受体识别,迅速调节宿主的促炎/抗炎平衡,增强对沙门氏菌的防御能力。
表4:家禽预防沙门氏菌的抗生素替代方案机制总结[td]| 替代品类别 | 典型代表成分 | 抗沙门氏菌的核心机制 | 应用优势 | | 益生菌 (Probiotics) | 枯草芽孢杆菌, 嗜酸乳杆菌 | 竞争性排斥结合位点;分泌乳酸及细菌素;直接杀菌或抑菌 | 建立健康的微生态平衡,改善饲料转化率 | | 益生元 (Prebiotics) | 甘露寡糖(MOS), 低聚果糖(FOS) | 作为靶向“诱饵”吸附病原菌;被有益菌发酵产生短链脂肪酸(SCFAs)促进肠绒毛发育 | 稳定性好,耐高温制粒,能特异性增强有益菌 | | 合生元 (Synbiotics) | 益生菌与益生元的联合配方 | 协同作用:益生元保障了益生菌在定植初期的营养和存活率 | 效力比单一添加更持久和显著 | | 后生元 (Postbiotics) | 灭活乳酸菌制剂, 酵母细胞壁提取物 | 直接提供免疫调节分子,迅速激活巨噬细胞,增强肠道紧密连接蛋白表达 | 零感染风险,极度耐热,化学性质极其稳定 |
6.3 噬菌体疗法 (Bacteriophage Therapy)
噬菌体是专门感染并裂解细菌的病毒。随着耐药性沙门氏菌的增加,噬菌体疗法迎来了复兴。- 优势: 噬菌体具有极高的宿主特异性(靶向裂解特定的沙门氏菌血清型),不会破坏肠道内正常的共生微生物群(无广谱抗生素带来的“菌群失调”副作用)。它们能够在定植位点自我复制扩增,且特别擅长穿透和破坏由沙门氏菌形成的难治性生物被膜。
- 挑战: 噬菌体极易受到胃酸的破坏(需要特殊的微囊化包被技术以实现肠道靶向释放),且沙门氏菌可能通过突变受体快速产生抗噬菌体抗性。目前通常采用“噬菌体鸡尾酒”(Phage cocktails,混合多种噬菌体)来克服抗药性问题。
6.4 农场生物安全与综合管理 (Biosecurity and Management)
即使有完善的疫苗和添加剂体系,如果没有严格的生物安全措施(Biosecurity),沙门氏菌的控制依然会功亏一篑。- 环境卫生: 实行严格的“全进全出”(All-in/All-out)饲养模式。空舍期间进行彻底的高压冲洗和甲醛/戊二醛熏蒸消毒。
- 病虫害控制: 建立坚固的防鼠网,使用杀虫剂消灭携带病菌的甲虫(特别是小黑甲)。
- 饮水管理: 对饮用水进行持续酸化或氯化处理,定期对管线进行除垢和生物被膜清除。
07结论与未来展望 (Conclusion and Future Perspectives)
沙门氏菌通过高度复杂的适应机制(如SPI-1和SPI-2致病岛)成功地在家禽体内确立了其生存地位,并使得家禽产品成为人类感染的持续来源。家禽自身的免疫系统,从先天性的TLRs受体识别到由Th1细胞介导的强大杀伤机制,构成了一张精密的防御网。然而,面对层出不穷的血清型变异和不断加剧的抗生素耐药性危机,依靠单一的“银弹”已经无法彻底解决家禽沙门氏菌问题。文献 (Shaji et al., 2023) 强调,未来的防控必须走“多管齐下的综合管理(One Health approach)”道路。这不仅要求研发出能够同时诱发强大粘膜免疫和细胞免疫、且不干扰血清学监测的新一代标志物疫苗(DIVA vaccines),同时也迫切需要深入破译家禽肠道微生物组的动态平衡密码,开发出更精准靶向的益生元、后生元和纳米微囊化噬菌体疗法。通过营养干预、遗传育种(选育抗病力强的品系)与顶尖的生物安全规范相融合,才能最终切断沙门氏菌从家禽农场到人类餐桌的传播链条,保障全球食品安全。
08参考文献 (References)- Shaji, S., Selvaraj, R. K., & Shanmugasundaram, R. (2023). Salmonella infection in poultry: A review on the pathogen and control strategies. Microorganisms, 11(11), 2814.
- Barrow, P. A., Jones, M. A., Smith, A. L., & Wigley, P. (2012). The long view: Salmonella-the last forty years. Avian Pathology, 41(5), 413-420.
- Gast, R. K., & Sharma, P. (2021). Salmonella infections. In D. E. Swayne et al. (Eds.), Diseases of Poultry (14th ed., pp. 719-753). Wiley-Blackwell.
- Foley, S. L., Nayak, R., Hanning, I. B., Tjellan, T. J., Han, J., & Ricke, S. C. (2011). Population dynamics of Salmonella enterica serotypes in US commercial peanut and poultry production systems. Applied and Environmental Microbiology, 77(13), 4273-4279.
- Wigley, P. (2014). Salmonella enterica in the chicken: how it has helped our understanding of immunology in a global food production animal. Frontiers in Immunology, 5, 482.
- Cheng, Y., Chen, Y., Li, X., et al. (2019). Immune responses of the avian immune system to Salmonella infection. Veterinary Immunology and Immunopathology, 218, 109941.
- Kogut, M. H., & Arsenault, R. J. (2017). Immunometabolic phenotype alterations associated with the induction of disease tolerance and persistent asymptomatic infection of Salmonella in the chicken. Frontiers in Immunology, 8, 372.
- Schneiders, G. H., et al. (2021). Bacteriophage therapy against Salmonella in poultry. Viruses, 13(5), 871.
- Ricke, S. C. (2021). Symposium review: prebiotics and probiotics as microbiome-targeted therapies for Salmonella in poultry. Poultry Science, 100(2), 856-865.
- Desin, T. S., K?ster, W., & Potter, A. A. (2013). Salmonella vaccines in poultry: past, present and future. Expert Review of Vaccines, 12(1), 87-96.
来源:菌中无戏言
|
|