|
|
马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
Joseph, J., et al., Avian Pathogenic Escherichia coli (APEC) in Broiler Breeders: An Overview. Pathogens, 2023. 12(11): p. 1280.
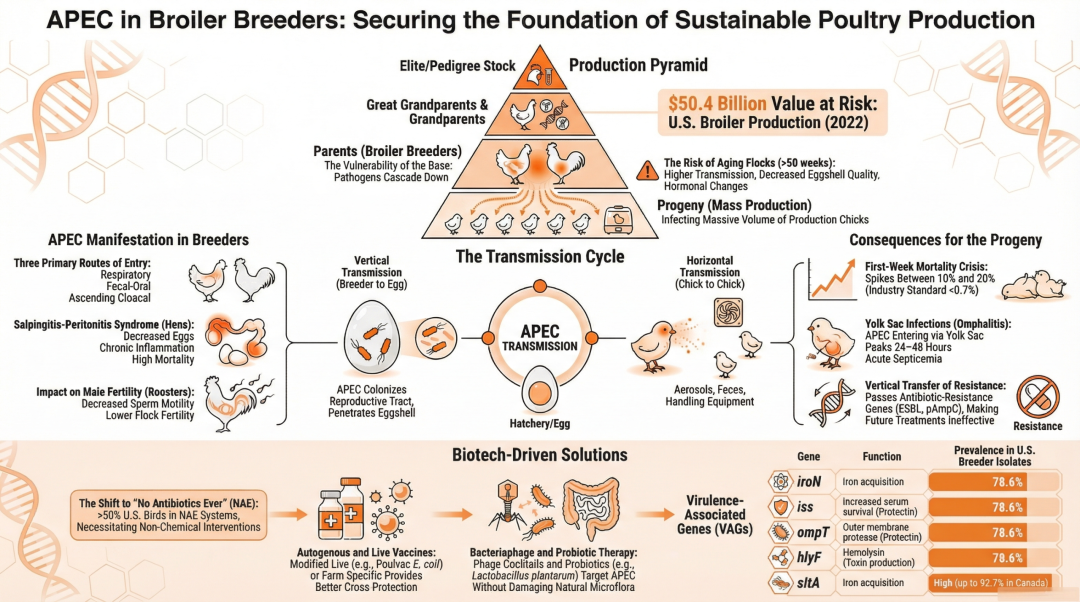
家禽产业在全球肉类和蛋类供应中占据着至关重要的地位,而肉鸡种鸡(Broiler Breeders)作为产业链的顶端,其健康状况直接决定了后代商品肉鸡的质量与生产性能。然而,禽致病性大肠杆菌(Avian Pathogenic Escherichia coli , APEC)引起的禽大肠杆菌病(Colibacillosis)一直是威胁肉鸡种鸡健康和家禽业经济效益的最具破坏性的细菌性疾病之一。APEC不仅会导致种鸡自身的严重疾病(如输卵管炎、卵黄性腹膜炎和败血症),还会通过垂直传播(Vertical Transmission)感染种蛋,导致胚胎死亡、孵化率下降以及初生雏鸡的卵黄囊感染。本文基于Joseph等(2023)的综述文献,深入探讨了APEC在肉鸡种鸡中的病原学特征、毒力因子、传播动力学、临床病理学、日益严峻的抗菌药物耐药性(AMR)挑战,以及当前的预防、控制和替代治疗策略。此外,本文还评估了APEC作为潜在的人兽共患病原体对公共卫生安全的威胁,旨在为家禽从业者、兽医和科研人员提供全面、前沿的理论参考。
一、引言
全球人口的持续增长推动了对优质动物蛋白需求的激增,家禽业因其高效的饲料转化率和相对较低的生产成本,成为满足这一需求的中坚力量。在这个庞大的产业金字塔中,肉鸡种鸡(Broiler Breeders)处于核心地位。种鸡群的健康、繁殖性能和免疫状态直接影响着数以亿计的商品肉鸡的产量和质量。然而,集约化、高密度的现代家禽养殖模式也为病原微生物的传播提供了温床。禽大肠杆菌病(Colibacillosis),由特定的大肠杆菌( Escherichia coli )致病株——即禽致病性大肠杆菌(APEC)引起,是全球家禽业面临的最普遍、最具经济破坏性的细菌感染之一 (Joseph et al., 2023)。在肉鸡种鸡中,APEC感染的后果尤为严重:它不仅导致成年种鸡的发病率和死亡率上升,严重损害其产蛋率和蛋品质,更致命的是,APEC能够定植于种鸡的生殖道,通过种蛋进行垂直传播。这种垂直传播机制导致后代雏鸡在孵化早期就面临极高的感染风险,表现为卵黄囊感染(Yolk sac infection)、脐炎和早期败血症,给家禽产业链造成了不可估量的经济损失。随着全球对抗菌药物使用的日益限制,以及多重耐药(MDR)APEC菌株的广泛出现,传统的抗生素治疗策略正面临巨大挑战。因此,深入理解APEC在肉鸡种鸡中的致病机制、传播途径,并开发有效的非抗生素干预策略,已成为当前兽医科学领域的紧迫任务。
二、APEC 的病原学特征与分型
2.1 病原学基础禽致病性大肠杆菌(APEC)属于肠杆菌科( Enterobacteriaceae ),是一种革兰氏阴性、兼性厌氧的杆状细菌。虽然大肠杆菌是人类和温血动物肠道微生物群落中的常见共生菌(Commensal bacteria),但APEC属于肠外致病性大肠杆菌(Extraintestinal Pathogenic E. coli , ExPEC)的一个重要分支。与肠道内共生的大肠杆菌不同,APEC获得了大量的毒力基因(Virulence genes),这些基因赋予了它们突破肠道黏膜屏障、在宿主血液和各种内部器官中存活、繁殖并引发系统性炎症的能力。
2.2 血清型与基因型多样性APEC菌株具有高度的遗传和抗原多样性。传统上,APEC的分类主要基于其表面抗原,包括O抗原(体细胞脂多糖)、K抗原(荚膜多糖)和H抗原(鞭毛蛋白)。在感染家禽的APEC中,某些特定的O血清群最为常见,其中 O1、O2 和 O78 是全球范围内公认的最主要的致病性血清群,占据了临床分离株的很大比例。然而,近年来随着全基因组测序(WGS)和多位点序列分型(MLST)技术的应用,研究表明仅靠血清型无法完全反映APEC的致病潜力。APEC的毒力往往是由位于质粒(Plasmids,如ColV和ColBM质粒)或染色体上的致病岛(Pathogenicity Islands, PAIs)上的特定毒力基因组合决定的。这使得APEC的诊断和疫苗开发变得极为复杂,因为不同血清型的菌株可能携带相似的毒力质粒,而同一血清型的菌株其致病力也可能存在巨大差异。
三、APEC 的核心毒力因子
APEC的致病性是一个极其复杂的多因素过程。为了在家禽体内成功建立感染并引发疾病,APEC必须具备一系列毒力因子。这些毒力因子协同作用,帮助细菌粘附于宿主细胞、获取生存必需的营养物质(如铁)、逃避宿主的免疫清除系统,并最终对宿主组织造成损伤。以下是对APEC关键毒力因子的详细分类与功能解析:
表1:肉鸡种鸡中APEC主要毒力因子及其致病机制毒力因子类别 | 具体的毒力因子/基因 | 基因名称 | 在APEC致病机制中的主要作用与功能描述 | 粘附素 (Adhesins)
| 1型菌毛 (Type 1 fimbriae) | fimC | 介导APEC最初粘附到家禽呼吸道上皮细胞,是定植的关键第一步。 | P型菌毛 (P fimbriae) | papC | 识别并结合宿主细胞表面的特异性糖脂受体,促进在内脏器官中的定植。 | 卷曲菌毛 (Curli) | csgA | 参与生物被膜(Biofilm)的形成,增强细菌在环境中的存活率和对宿主组织的附着力。 | 温度敏感性血凝素 | tsh | 存在于大质粒上,不仅具有粘附功能,还可能具有蛋白酶活性,促进组织侵袭。 | 铁获取系统 (Iron Acquisition)
| 气杆菌素 (Aerobactin) | iucD, iutA | 强效的铁载体,在宿主体内缺铁环境中高效螯合铁离子并转运入细菌细胞内,对APEC在血清中存活至关重要。 | 肠杆菌素 (Enterobactin) | entB | 另一种常见的铁载体,帮助细菌从宿主转铁蛋白中竞争性地获取铁。 | 沙门菌素 (Salmochelin) | iroN | 一种经过糖基化修饰的肠杆菌素,能够逃避宿主脂质运载蛋白(Lipocalin-2)的结合与中和。 | 耶尔森菌素 (Yersiniabactin) | ybtA | 在系统性感染和呼吸道定植中发挥重要作用的高亲和力铁载体。 | 保护素/血清抗性 (Protectins)
| 荚膜 (Capsule, K1等) | kpsMT II | 形成物理屏障,保护细菌免受宿主吞噬细胞的吞噬以及补体系统的杀伤。 | 增加血清存活蛋白 (Iss) | iss | 定位于外膜,显著增强APEC抵抗宿主血清补体经典和替代途径杀伤的能力。 | 外膜蛋白A (OmpA) | ompA | 维持细菌细胞膜的完整性,并参与抵抗宿主免疫系统的攻击。 | 毒素 (Toxins) | 溶血素 (Hemolysin) | hlyA | 破坏宿主红细胞及其他细胞的细胞膜,释放铁和其他营养物质供细菌利用。 |
| 空泡形成自身转运毒素 | vat | 一种细胞毒素,可引起宿主细胞内空泡化,导致细胞死亡和组织损伤。 |
| 分泌型自身转运毒素 | sat | 破坏宿主细胞的紧密连接,增加细胞通透性,促进细菌的侵袭和扩散。 |
3.1 粘附与定植:感染的先决条件感染的第一步是细菌在宿主黏膜表面的粘附。APEC通过表达多种菌毛(Fimbriae)和非菌毛粘附素来实现这一点。1型菌毛( fimC )在识别甘露糖受体方面发挥重要作用,是APEC在气管和呼吸道定植的关键。在种鸡的生殖道感染中,特定的粘附素也帮助细菌附着于输卵管上皮细胞,为垂直传播创造条件。
3.2 铁获取机制:营养竞争的武器铁是大多数细菌生存和增殖不可或缺的微量元素。然而,在禽类宿主(如血液、输卵管液)中,游离铁的浓度极低,大部分铁被结合在转铁蛋白等宿主蛋白中。APEC拥有高度发达的铁摄取系统(Iron uptake systems),包括气杆菌素(Aerobactin)和沙门菌素(Salmochelin)。这些系统构成了APEC的核心毒力质粒库(如ColV质粒),使得APEC能够在宿主体内的极端“缺铁”环境中成功繁衍。
3.3 逃避宿主免疫:血清抗性与保护素进入血液循环后,APEC必须抵御宿主的固有免疫系统,特别是血清中的补体系统和吞噬细胞(如巨噬细胞和异嗜性粒细胞)。 iss (增加血清存活率)基因被认为是APEC最重要的毒力标志之一,它通过抑制补体级联反应的末端复合体形成,使APEC具备强大的抗血清杀伤能力。此外,K1荚膜多糖不仅能提供物理保护,还能通过模拟宿主自身抗原实现“免疫伪装”。
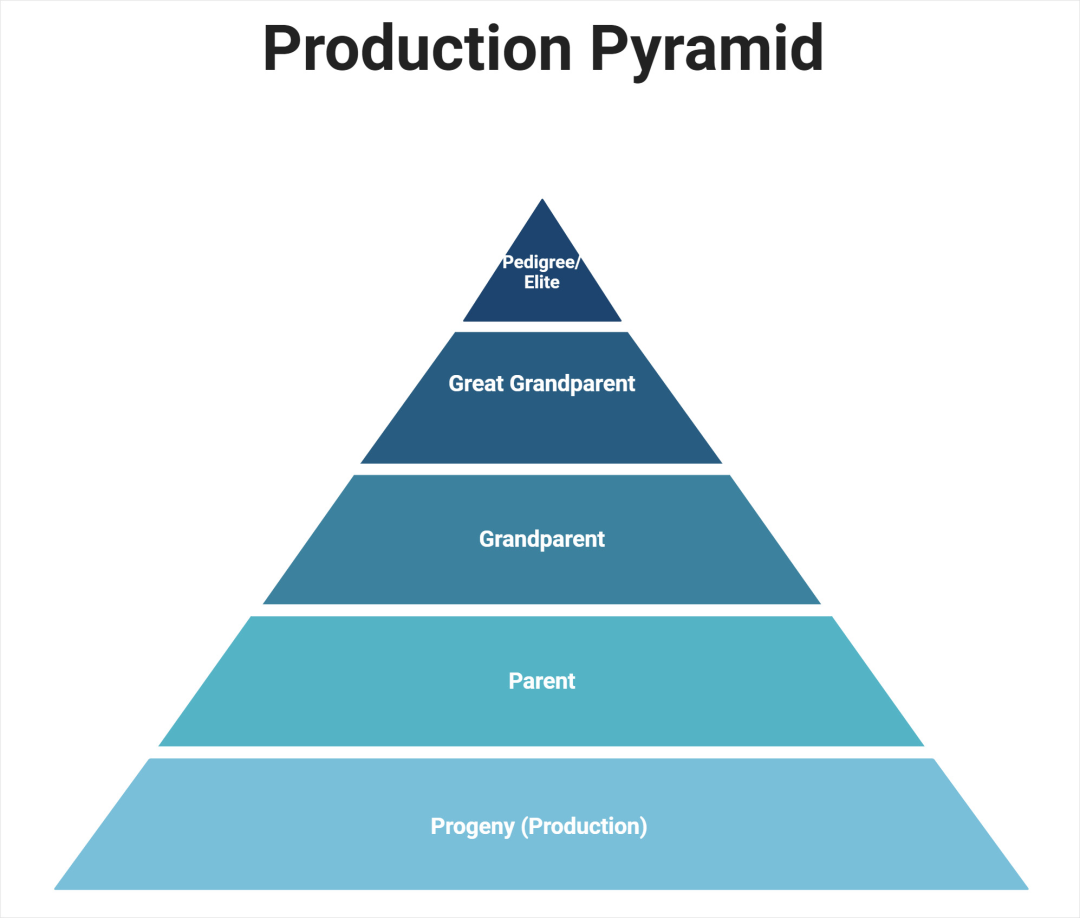
图1. 展示家禽产业生产金字塔的示意图。金字塔的最高层级为精英或血统组,最低层级为后代或生产农场。
四、传播途径的复杂性
在肉鸡种鸡群中,APEC的传播途径极其复杂,涵盖了环境到个体的水平传播,以及亲代到子代的垂直传播。这两种传播模式相互交织,构成了APEC在现代家禽生产系统中难以根除的传播网络。
4.1 水平传播 (Horizontal Transmission)
水平传播是APEC在鸡群内部和鸡群之间传播的主要方式。- 呼吸道途径: APEC通常存在于鸡舍的灰尘、羽毛碎屑和干燥的粪便中。当舍内通风不良、氨气浓度过高时,种鸡呼吸道纤毛的清除功能受损,吸入含有APEC的气溶胶后,细菌极易在呼吸道定植,随后侵入气囊引起气囊炎(Air sacculitis),并最终进入血液导致败血症。
- 粪口途径与环境污染: APEC从感染鸡的粪便中大量排出,污染饲料、饮水和垫料。健康鸡只通过啄食或饮水摄入病原体。
- 交配与生殖道感染: 对于肉鸡种鸡而言,自然交配或人工授精过程是水平传播的另一个重要途径。公鸡的泄殖腔如果携带APEC,可以直接将细菌引入母鸡的阴道和输卵管,导致严重的生殖道感染。
4.2 垂直传播 (Vertical Transmission)
这是肉鸡种鸡面临的最独特也最危险的传播方式。垂直传播意味着APEC可以直接从被感染的母鸡传递给种蛋,进而感染孵化出的雏鸡。- 经卵巢/输卵管感染 (Infection of the ovary/oviduct): 当种鸡发生系统性APEC感染或局部的卵黄性腹膜炎/输卵管炎时,细菌可以在卵子形成或蛋壳沉淀的过程中,直接进入卵黄、蛋清或蛋壳膜内部。这种内部污染的种蛋在孵化过程中,胚胎几乎无法存活,或者孵化出带有严重卵黄囊感染的弱雏。
- 蛋壳表面污染后渗透: 被带有APEC的粪便污染的产蛋箱,会导致新产出的种蛋表面附着大量病原体。由于蛋壳在产出时表面湿润且具有微孔,当蛋在冷却过程中内部压力降低时,表面的APEC会随着水分被“吸入”蛋壳内部,造成二次污染。
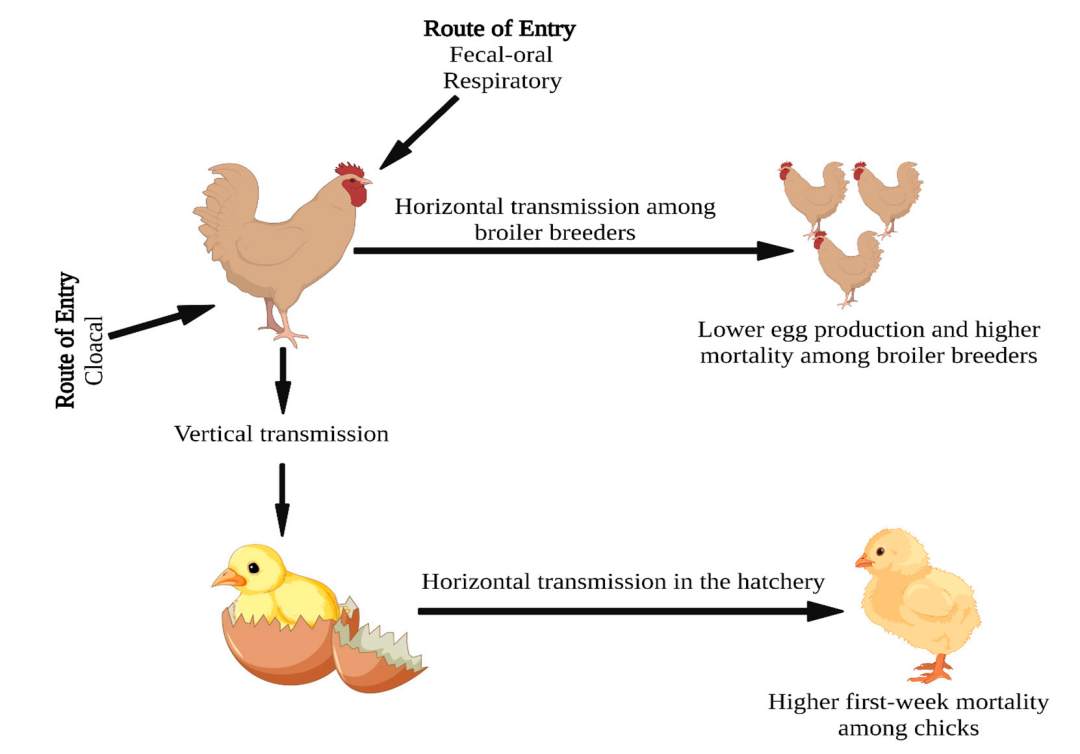
图2. 展示APEC入侵途径、向雏鸡的垂直传播以及在孵化场和肉鸡种鸡间水平传播的图像。
五、临床症状与病理学特征 APEC
引起的禽大肠杆菌病并不是一种单一的疾病,而是一系列局部和系统性感染的综合征。在肉鸡种鸡和它们的后代中,临床表现存在显著差异。
5.1 成年肉鸡种鸡的临床表现
在成年种鸡中,APEC感染往往表现为慢性或亚急性经过,对生产性能的打击是毁灭性的:- 输卵管炎 (Salpingitis) 与卵黄性腹膜炎 (Egg Peritonitis): 这是母鸡最典型的病变。APEC感染输卵管会导致其发炎、肿胀,内部蓄积大量干酪样渗出物(俗称“蛋中蛋”样病变)。当卵泡破裂或输卵管功能丧失时,卵黄物质落入腹腔,引发严重的卵黄性腹膜炎。病鸡表现为腹部膨大、企鹅样站立姿势、停止产蛋,并最终死于毒血症或败血症。
- 蜂窝织炎 (Cellulitis): 主要发生在下腹部或腿部皮肤下方。常由于抓伤等皮肤破损感染APEC引起,表现为皮下组织内形成坚硬的、黄色的干酪样斑块。
- 急性败血症 (Acute Septicemia): 在应激或合并感染(如传染性支气管炎病毒、支原体)的情况下,APEC迅速在血液中繁殖。病死鸡解剖可见典型特征: 心包炎 (Pericarditis) (心包膜增厚,内有纤维素性渗出)、 肝周炎 (Perihepatitis) (肝脏表面覆盖一层白色或灰色的纤维素性伪膜)以及 气囊炎 (Air sacculitis) 。
5.2 对子代(初生雏鸡)的影响
垂直传播的后果集中体现在孵化阶段和育雏的第一周:- 胚胎死亡率增加: 受感染的种蛋通常在孵化中后期出现胚胎死亡。
- 卵黄囊感染与脐炎 (Yolk Sac Infection & Omphalitis): 这是商品肉鸡生产中最常见的首周死亡原因。病雏表现为腹部膨大、脐带愈合不良且有恶臭(“糊肛”)。解剖可见卵黄囊异常变大,卵黄液变得稀薄呈水样,或变成粘稠的干酪样物质,血管充血。这些雏鸡即使存活,其生长发育也会严重受阻。
六、诊断与监测
准确诊断APEC感染对于及时采取干预措施至关重要。- 病原分离与鉴定: 传统的“金标准”是从患病禽类典型的内脏病变部位(如心包液、肝脏表面、受感染的卵黄囊或输卵管渗出物)进行无菌采样,接种于麦康凯琼脂(MacConkey agar)上。APEC通常表现为发酵乳糖的粉红色菌落。
- 生化鉴定: 使用常规生化测试或现代的生化鉴定系统(如API 20E或VITEK)确认其大肠杆菌身份。
- 分子生物学诊断(PCR): 由于健康鸡的肠道中也存在非致病性的大肠杆菌,因此仅仅分离出大肠杆菌是不够的。目前兽医诊断实验室广泛采用多重聚合酶链反应(Multiplex PCR)技术。通过检测前文提到的特定毒力基因(如 iss, tsh, iucD, cvi/cva, papC 等)组合,将分离株明确鉴定为禽致病性大肠杆菌(APEC),并评估其致病潜力。
七、抗菌药物耐药性
在过去的几十年里,为了控制大肠杆菌病,全球家禽业严重依赖预防性和治疗性抗生素的使用。这种长期的选择性压力导致了APEC中多重耐药性(MDR)菌株的广泛出现,这不仅直接导致临床治疗失败率上升,更是全球公共卫生面临的重大威胁 。
表2:APEC中常见的抗生素耐药机制与相关基因| 抗生素类别 | 常见耐药基因 (Resistance Genes) | 具体的耐药分子机制 | 在APEC中的流行情况及危害 | | β-内酰胺类 (含头孢菌素类) | blaTEM, blaCTX-M, blaSHV | 产生超广谱β-内酰胺酶(ESBLs),水解破坏抗生素分子结构中的β-内酰胺环。 | 极度普遍。ESBL-APEC的出现使得氨苄西林和第三代头孢菌素(重要的人类临床用药)在家禽中失效。 | | 四环素类 (Tetracyclines) | tet(A), tet(B) | 主要通过主动外排泵(Efflux pumps)将药物排出细胞外,或产生核糖体保护蛋白。 | 在全球各地的APEC分离株中,对四环素的耐药率通常是最高的(常超过80%)。 | | 氨基糖苷类 (Aminoglycosides) | aadA, strA, strB, aph | 产生氨基糖苷类修饰酶(如乙酰转移酶、磷酸转移酶),使药物失去与核糖体结合的能力。 | 常见于肉鸡和种鸡群体,导致链霉素、庆大霉素治疗效果显著下降。 | | 磺胺类与甲氧苄啶 | sul1, sul2, dfrA | 编码对药物具有低亲和力的二氢叶酸合成酶或还原酶,绕过药物的代谢阻断。 | 广泛分布于各类质粒和整合子(Integrons)中,极易在菌株间发生水平基因转移。 | | 氟喹诺酮类 (Fluoroquinolones) | gyrA, parC 突变, qnr基因 | 靶位(DNA促旋酶或拓扑异构酶)基因发生点突变;或通过质粒介导的抗性(PMQR)。 | 严重威胁。恩诺沙星等曾是治疗大肠杆菌病的特效药,现耐药率急剧上升。 | | 多粘菌素 (Colistin) | mcr-1, mcr-2 等 | 磷酸乙醇胺转移酶修饰脂多糖(LPS)结构(Lipid A),降低细菌膜对多粘菌素的亲和力。 | 极度危险! 多粘菌素被视为人类抗感染的“最后防线”。质粒介导的mcr基因在家禽APEC中的传播引发了全球公共卫生危机。 |
7.1 耐药基因的水平转移 (Horizontal Gene Transfer)
APEC之所以成为耐药基因的超级载体,在于这些耐药基因大多位于移动基因元件(Mobile Genetic Elements, MGEs)上,如质粒(Plasmids)、转座子(Transposons)和整合子(Integrons)。这使得APEC不仅能在自身菌株间传递耐药性,还能将耐药基因传递给肠道内的其他致病菌(如沙门氏菌)甚至人类致病菌。
7.2 Colistin (多粘菌素) 耐药性的危机
特别值得一提的是,多粘菌素被世界卫生组织(WHO)列为治疗人类严重多重耐药革兰氏阴性菌感染的“最高优先级极重要抗菌药物”。然而,由于过去多粘菌素在家禽业中作为促生长剂或治疗药物的广泛使用,导致了通过质粒介导的 mcr-1 基因的产生。带有 mcr-1 基因的APEC在家禽中的流行,彻底打破了多粘菌素作为最后防线的安全性,成为当前“同一健康”(One Health)概念下亟待解决的核心问题。
八、预防、控制与替代治疗策略
鉴于抗生素使用的严格限制(如全球多国推行的“无抗养殖”政策),肉鸡种鸡场必须采取综合性、前瞻性的管理策略来对抗APEC 。
8.1 严格的生物安全与环境管理 (Biosecurity and Management)
控制APEC的首要步骤是切断传播途径,特别是水平传播:- 孵化场与种蛋管理: 保持产蛋箱的绝对清洁,增加收集种蛋的频率,防止种蛋在鸡舍内受到粪便污染。坚决淘汰地面蛋和明显脏污的种蛋,不进行孵化。对合格种蛋进行科学的熏蒸消毒。
- 环境卫生: 优化鸡舍通风,降低粉尘和氨气浓度,这能显著降低种鸡呼吸道黏膜的损伤,从而降低APEC的气源性感染风险。提供清洁的饮水,定期对水线进行酸化和消毒,防止水线生物被膜的形成。
8.2 疫苗接种 (Vaccination)
对于价值极高的肉鸡种鸡而言,免疫接种是提供特异性保护的关键手段。- 灭活疫苗 (Bacterins / Inactivated Vaccines): 通常根据农场或地区分离到的特定APEC菌株(如O78)定制生产(自家苗,Autogenous vaccines)。其优点是安全性高,缺点是只能提供同源血清型的保护,且通常需要多次注射才能维持长期的抗体水平。
- 活毒减毒疫苗 (Live Attenuated Vaccines): 如商品化的Poulvac? E. coli 疫苗。这类疫苗可以通过喷雾或饮水方式大批量接种。它们能有效激发黏膜免疫和细胞免疫反应,不仅能在一定程度上提供针对不同血清型(异源)的交叉保护,还能通过竞争性排斥减少环境中野毒株的载量。在种鸡中应用疫苗,不仅能保护母鸡免受输卵管炎的侵害,还能通过母源抗体(Maternal antibodies)传递给蛋黄,为初生雏鸡提供早期保护。
8.3 非抗生素替代疗法的前沿进展
随着“后抗生素时代”的逼近,科学界正大力研发针对APEC的新型干预措施:
表3:肉鸡种鸡中APEC的非抗生素替代防治策略总结| 替代疗法类别 | 作用机制与优势 | 当前应用与研究进展 (Joseph et al., 2023 总结) | | 益生菌 (Probiotics) | 通过竞争性排斥(占据肠道结合位点)、产生短链脂肪酸降低肠道pH值、分泌细菌素(Bacteriocins)直接抑制APEC,并调节宿主局部免疫。 | 常用的包括乳酸杆菌、芽孢杆菌和双歧杆菌。在雏鸡日粮中添加可显著降低肠道内APEC的定植率和发病率。 | | 噬菌体疗法 (Bacteriophage Therapy) | 噬菌体是专门感染并裂解细菌的病毒。具有高度的宿主特异性,不会破坏肠道正常菌群。对多重耐药APEC同样有效。具有巨大的商业潜力。 | 研究表明,噬菌体鸡尾酒(Phage cocktails)可通过气雾或饮水投喂,有效降低败血症死亡率。 | | 抗菌肽 (Antimicrobial Peptides, AMPs)(如文献提及的cLF36, D-CATH-2) | 广泛存在于宿主先天免疫系统中,带正电荷,通过静电吸引直接破坏细菌带负电荷的细胞膜。不易产生耐药性 (Mahlapuu et al., 2016)。 | Cuperus等 (2016) 以及 Daneshmand等 (2019) 证明,胚内注射(in ovo)或饲料添加特定AMPs可保护雏鸡免受致死性APEC攻击,改善肠道形态。 | | 抗毒力药物 (Anti-virulence Drugs) | 不直接杀死细菌(从而降低选择压力),而是特异性靶向细菌的毒力因子,如抑制菌毛的组装或阻断铁获取系统。 | Totsika (2017) 指出,这是一种极具前景的新型策略。通过“解除细菌武装”使其失去致病力,等待宿主自身免疫系统清除病原体。 | | 卵内注射技术 (In ovo Administration) | 在孵化期的特定阶段(通常为第18天,转移到出雏器时),将免疫刺激剂、疫苗或AMPs直接注射到种蛋的羊膜腔内。 | Dar (2018) 研究证实,通过卵内接种先天免疫刺激剂,可以极大地保护初生雏鸡免受致命的卵黄囊感染和早期死亡。 |
九、APEC 的人兽共患潜力 (Zoonotic Potential) 与公共卫生安全
这篇文献(Joseph et al., 2023)深刻指出了APEC超越家禽疾病范畴的重要属性:其作为潜在的人兽共患病原体对人类健康的威胁。
比较基因组学研究揭示,分离自家禽的APEC与引起人类肠外感染的大肠杆菌(Human ExPEC)——特别是引起人类尿路感染的 尿道致病性大肠杆菌 (UPEC)和引起新生儿脑膜炎的大肠杆菌(NMEC) ——在基因组层面存在惊人的高度相似性。它们共享了大量的毒力基因、致病岛和携带这些基因的大型毒力质粒。
这种相似性带来了两个重大的公共卫生担忧:- 直接感染潜力: 某些APEC菌株可能作为“潜在的”人兽共患病原体,通过食物链(如消费未煮熟的污染禽肉或接触被污染的环境)直接感染人类,引发尿路感染或更严重的败血症。
- 基因库的角色: 即便APEC本身不直接感染人类,家禽作为巨大的“孵化器”,其体内的APEC可以作为毒力基因和多重耐药基因的庞大储库(Reservoir)。通过质粒的水平转移,APEC能够将其“最致命”和“最耐药”的基因武器传递给人类肠道内的共生大肠杆菌或人类致病菌,极大地恶化了人类感染的治疗困境。
十、结论
综上所述,禽致病性大肠杆菌(APEC)在肉鸡种鸡中的存在,不仅是对家禽业经济效益的重大打击,引发严重的生产性能下降和高死亡率的卵黄囊感染,更是一场正在演变的公共卫生危机。由于其极其复杂的毒力机制、多样化的血清型以及不可阻挡的多重耐药性进化趋势,单纯依靠传统的抗生素干预已经难以为继。未来的应对策略必须基于“同一健康”(One Health)的宏大视角,在以下几个方面取得突破:第一,不断优化肉鸡种鸡群和孵化场的生物安全管理,从源头切断垂直和水平传播;第二,加速开发广谱、高效的新型多价疫苗,为种鸡及其子代构建坚固的免疫屏障;第三,积极推进如抗菌肽、噬菌体、益生菌和抗毒力药物等非抗生素替代疗法的商业化应用。只有综合运用这些前沿策略,才能在保障全球家禽产品安全供给的同时,有效遏制耐药基因的蔓延,保护人类免受潜在人兽共患病原的威胁。
来源:菌中无戏言,作者:凤凰于飞
|
|