|
|
马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
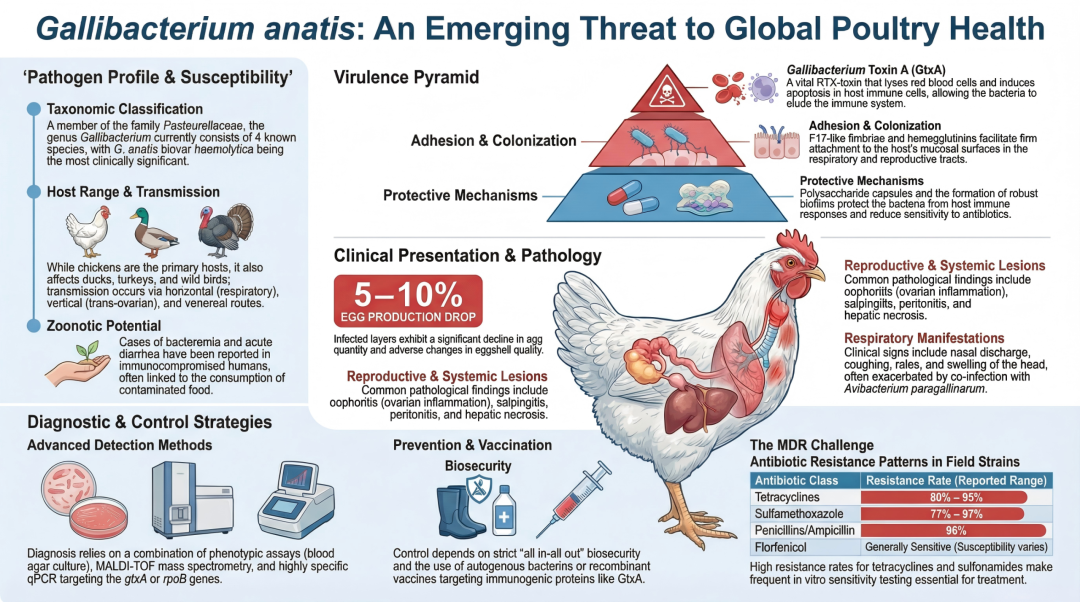
原文标题: Gallibacterium anatis infection in poultry: a comprehensive review
原文出处: Tropical Animal Health and Production (2023) 55:383
作者: Wafaa A. Abd El-Ghany, Abdelazeem M. Algammal, Helal F. Hetta, Ahmed R. Elbestawy
发表日期: 2023年10月27日
01摘要 (Abstract)
鸭源鸡杆菌( Gallibacterium anatis ,简称 G. anatis )是巴斯德菌科(Pasteurellaceae)的一员,通常作为正常菌群栖息于家禽的上呼吸道和下生殖道中。然而,在免疫抑制、混合感染(特别是与大肠杆菌或支原体混合感染)或各种应激因素存在的特定情况下, G. anatis 会引起呼吸道、生殖道及全身性疾病。
目前, G. anatis 感染已在全球多个国家出现。该细菌主要感染鸡,但其他种类的家禽和野生鸟类也可能被感染。已有报告证实了 G. anatis 的水平传播、垂直传播和性传播途径。 G. anatis 的致病性主要与一些关键的毒力因子有关,如鸡杆菌毒素 A(Gallibacterium toxin A, GtxA)、菌毛(fimbriae)、血凝素(haemagglutinin)、外膜囊泡(outer membrane vesicles)、荚膜(capsule)、生物膜(biofilms)和蛋白酶(protease)。
G. anatis 感染的临床表现主要特征为气管炎、卵巢炎、输卵管炎和腹膜炎,而在伴发感染的情况下可能会注意到其他病变。控制这种感染主要依赖于实施生物安全措施和疫苗接种。药敏试验对于 G. anatis 的正确治疗是必要的。然而,多重耐药性(MDR)的发展非常普遍。本综述文章从历史、易感性、传播、毒力因子、发病机制、临床表现、诊断及防控措施等方面对 G. anatis 进行了阐述。
02引言 (Introduction)
家禽的某些感染对产蛋量有巨大的直接负面影响,或对家禽的健康状况产生间接影响。其中一种细菌感染就是鸭源鸡杆菌( G. anatis )感染。 G. anatis 是巴斯德菌科的一员。1981年,巴斯德菌科的分类学得以确立,该科主要由从动物分离的革兰氏阴性球杆菌组成。迄今为止,该科包括15个属,其中包括巴斯德氏菌属( Pasteurella )、禽杆菌属( Avibacterium )、放线杆菌属( Actinobacillus )和鸡杆菌属( Gallibacterium )等。
根据多项研究,鸡杆菌属可导致家禽甚至人类死亡,这表明其危害性超过了普通的机会性感染。长期以来,由于对发病机制、毒力和生长动力学的理解不完全, G. anatis 的重要性被低估了。然而,近年来在蛋鸡、种鸡和肉鸡群中, G. anatis 疾病的总发病率有所上升。如今,这种新出现的疾病对世界鸡肉和蛋类产业构成了严重威胁。
该病广泛分布于美洲、欧洲、澳洲、非洲和亚洲国家。尽管在特定环境和应激条件下, G. anatis 可被视为下生殖道、消化道末端和上呼吸道正常微生物群的一部分,但它会引发家禽的生殖和全身性疾病。包括人类在内的家禽和非家禽物种以及哺乳动物都对 G. anatis 感染易感。
该细菌具有多种毒力因子,特别是在存在合并感染和其他与环境条件相关的应激源时,会导致生殖和呼吸组织损伤。 G. anatis 感染可引起局部或全身性影响,通常伴随着产蛋性能显著下降、产蛋率下降5-10%、蛋壳质量恶化、死亡率增加、呼吸道表现和腹泻。卵巢炎、输卵管炎、附睾炎、腹膜炎、败血症、呼吸道病变、肠炎、肝坏死和心包炎是 G. anatis 感染最常见的病变。
为了快速检测 G. anatis 感染,除了常规的培养或生化表型测定外,还采用了现代先进的诊断和鉴定技术。尽管 G. anatis 对许多抗菌药物敏感,但有些病例无反应,并且已有疾病复发的报告。多重耐药性(MDR)的发展、显著的抗原变异以及宿主无法有效清除 G. anatis 是疾病控制的主要限制因素。广泛的抗生素耐药性导致治疗无效。 G. anatis 菌株的抗生素敏感性不断变化,因此,频繁的体外菌株评估至关重要。目前仅有少数疫苗被开发用于对抗 G. anatis 并正在接受评估。
03历史 (History)- 1950年: G. anatis 首次被发现是作为外观健康鸡泄殖腔正常微生物群的一部分,当时被称为“溶血性泄殖腔细菌”(hemolytic cloaca bacterium)。
- 分类学演变: 后来,DNA杂交技术表明,禽溶血性巴斯德氏菌( Pasteurella hemolytica )、输卵管炎放线杆菌( Actinobacillus salpingitidis )和鸭巴斯德氏菌( P. anatis )属于巴斯德菌科内的不同属。
- 2003年: Christensen等人将鸡杆菌属( Gallibacterium )分类为一个单独且独立的属。分类单元1(Taxon 1),即被标记为鸭巴斯德氏菌( P. anatis )的第3组菌株,与输卵管炎放线杆菌和禽溶血性巴斯德氏菌密切相关。
- 当前分类: 根据16S rRNA基因序列,禽溶血性巴斯德氏菌随后被重新分类为 G. anatis 溶血生物型(biovar hemolytica)。目前,该属包括4个已知种:
- G. anatis (包括溶血生物型和鸭生物型)
- G. salpingitidis
- G. melopsittaci
- G. trehalosi fermentans 以及3个基因种(1、2和3)和未命名的第V组。
细菌特征: G. anatis 是一种革兰氏阴性、多形态、有荚膜、无运动性、不形成芽孢的兼性厌氧细菌(在补充有5-10%二氧化碳的血琼脂培养基上生长需要微需氧条件)。在表型上, G. anatis 分为产生β-溶血的“溶血”生物型(biovar haemolytica)和不产生溶血变异的“鸭”生物型(biovar anatis)。
全球分布: 该病已在多个大洲出现,包括欧洲(德国、丹麦、奥地利、英国、挪威、瑞典、捷克共和国、罗马尼亚)、美洲(美国、加拿大、墨西哥、巴拿马、秘鲁)、澳洲(澳大利亚)、非洲(尼日利亚、埃及、摩洛哥)和亚洲(日本、中国台湾、中国大陆、印度、伊朗、土耳其、叙利亚)。
表 1:全球 G. anatis 感染的首次检测、发生率和诊断方法(2003年新分类建立后)| 大洲 | 国家 | 禽类类型 | 采集器官 | 诊断方法 | 发生率 (%) | 参考文献 | | 非洲 | 埃及 | 蛋鸡 | 气管、卵巢和输卵管 | 表型鉴定、cPCR和测序 | 13.1 | Elbestawy (2014) | | 尼日利亚 | 疣鼻栖鸭 (Muscovy ducks) | 气管和泄殖腔拭子及卵巢组织 | 表型鉴定 | 33.2 | Lawal et al. (2017) |
| | 摩洛哥 | 蛋鸡 | 卵巢、气管和泄殖腔 | 表型鉴定和cPCR | 100 | Nassik et al. (2019) |
| | 欧洲 | 丹麦 | 蛋鸡和种鸡 | 气管和泄殖腔 | 表型鉴定和cPCR | 28.8 | Christensen et al. (2003); Bojesen et al. (2003a, b) | | 奥地利 | 蛋鸡 | 输卵管 | 表型鉴定 | 96.7 | Neubauer et al. (2007) |
| | 波兰 | 孔雀 | 肺 | 表型鉴定 | 5 | Rzewuska et al. (2007) |
| | 罗马尼亚 | 后院鸡群 | 卵巢、肺、心脏和脾脏 | 表型鉴定 | 3.3 | Sorescu et al. (2021) |
| | 亚洲 | 中国 | 蛋鸡 | 输卵管、卵巢、肝、脾和上呼吸道 | 表型鉴定和cPCR | 100 | Chuan-qing et al. (2008) | | 印度 | 鸭、鸽、肉鸡和蛋鸡 | 心血、脾脏和气管拭子 | 表型鉴定和cPCR | 100 | Singh et al. (2018) |
| | 土耳其 | 蛋鸡 | 气管、肺、肝和心脏 | 表型鉴定和cPCR | 2.2 | Yaman and Sahan (2019) |
| | 伊朗 | 蛋鸡 | 卵巢、输卵管、子宫、泄殖腔和腹腔 | 表型鉴定和cPCR | NA | Ataei et al. (2017) |
| | 澳洲 | 澳大利亚 | 蛋鸡 | 泄殖腔和输卵管 | 表型鉴定 | 55.5–100 | Shini et al. (2013) | | 北美洲 | 美国 | 蛋鸡 | NA | 表型鉴定、cPCR和测序 | NA | Johnson et al. (2011) | | 肉鸡和种鸡 | 关节、肉垂、肺、腹部和心脏 | 表型鉴定、cPCR和测序 | NA | Jones et al. (2013) |
|
| | 墨西哥 | 未成熟肉种鸡、种鸡、肉鸡、蛋鸡 | 肝、输卵管、卵巢、关节、骨、肺、心包和脾脏 | 表型鉴定 | NA | Shapiro et al. (2013) |
| | 蛋鸡 | 肺、气管、卵巢 | 表型鉴定和cPCR | 76.6 | Castellanos et al. (2006); Chavez et al. (2017a) |
|
| | 巴拿马 | 种鸡 | NA | 表型鉴定和血清学 | NA | Calderon and Thomas (2009) |
| | 南美洲 | 秘鲁 | NA | NA | 16S rRNA基因序列的限制性内切酶分析 | NA | Mendoza et al. (2014) |
(注:NA 代表数据不可用)
04易感性 (Susceptibility)
G. anatis 的宿主范围非常广泛:- 家禽与野生鸟类: 鸡、鸭、鹅、火鸡、鸽子、野鸡、珍珠鸡、虎皮鹦鹉、孔雀、鹦鹉、鹧鸪、牛背鹭、蹼足鸡形目鸟类、鹦鹉科鸟类和猫头鹰。
- 年龄易感性: 早期研究认为幼鸟比成年鸟易感性低,但近期研究(Huangfu et al., 2012)显示在5-6周、12周、18周和55-58周龄的鸡中检测率极高。此外,肉鸡中也分离出了该菌。
05感染与传播 (Infection and Dissemination)
- 水平传播: 主要途径是通过呼吸道进行。因此,该细菌主要流行于生物安全措施水平较低的鸡群中。
- 系统性传播: 从身体不同器官分离出 G. anatis 表明该细菌可从其自然栖息地进入体循环并扩散。
- 上行性感染: 生殖器官的感染可能与来自泄殖腔的上行性感染有关。
- 垂直传播: 实验证据表明存在垂直传播,途径包括经卵巢/输卵管途径或经蛋壳途径。 G. anatis 可在感染后10天的蛋黄和卵巢中分离到。在受精卵中,细菌可穿透蛋壳气孔感染发育中的胚胎并导致死亡。
- 性传播(Venereal transmission): 已有建议提出性传播的可能性,因为 G. anatis 会损害精液质量并引起附睾炎。感染公鸡的精液可能在成年鸟之间传播,并可能传播给后代。公鸡鼻内接种 G. anatis 后,一周内即可在睾丸和附睾中发现病原体。
06人兽共患重要性 (Zoonotic Importance)
据推测, G. anatis 是一种可传播给人类的食品污染物。- 首例报告: 2013年,法国报告了首例由 G. anatis 引发的菌血症,患者为一名免疫功能低下的女性,通过食用受污染的食物感染。主要症状包括发烧、严重腹痛、贫血、腹泻和中性粒细胞减少症。
- 近期案例: Wang et al. (2023) 报告了一例由 G. anatis 引起的急性水样腹泻病例,患者为一名患有2型糖尿病和高血压的62岁男性,症状仅表现为恶心和呕吐。
07毒力因子 (Virulence Factors)
G. anatis 拥有一系列复杂的毒力因子,使其能够粘附、定植、逃避免疫系统并造成组织损伤。
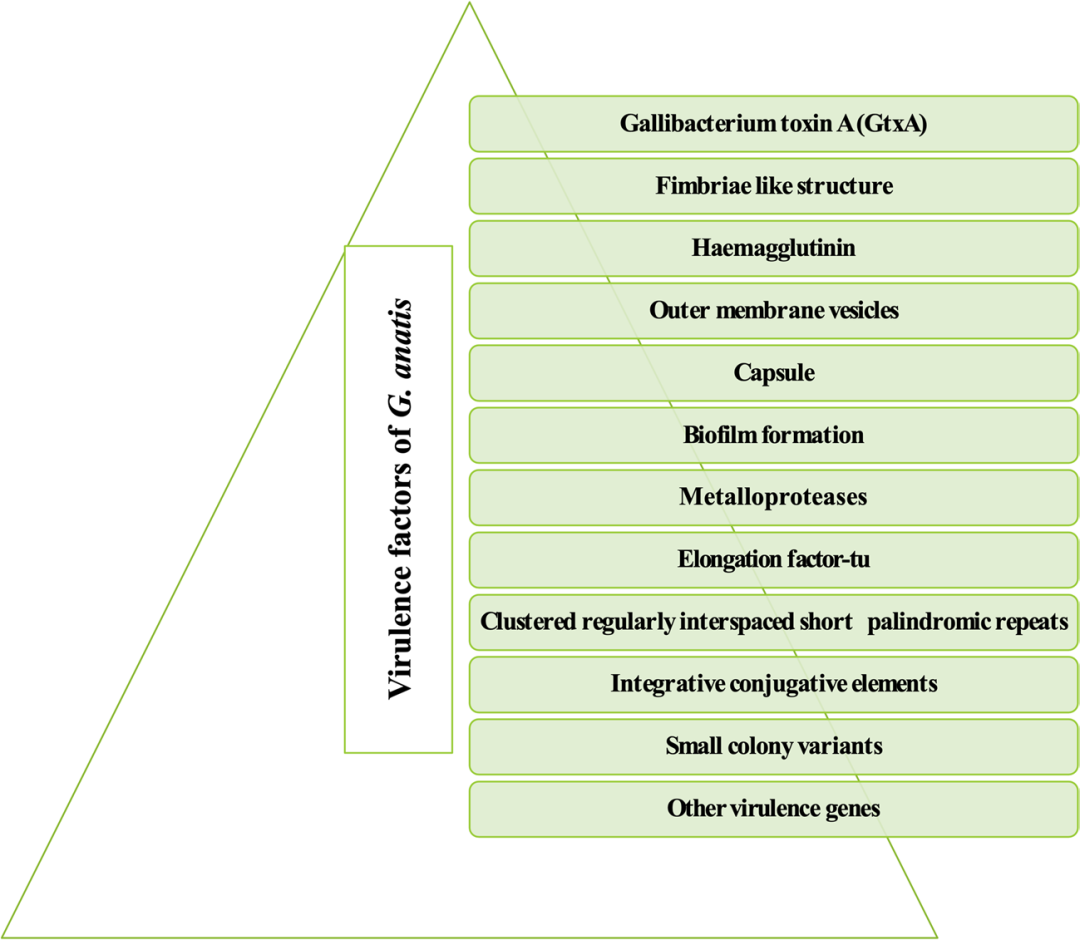
图 1: G. anatis 溶血生物型的毒力因子 (Virulence factors of G. anatis biovar haemolytica)
- 鸡杆菌毒素 A (Gallibacterium toxin A, GtxA):
- 这是 G. anatis 溶血生物型负责溶血特性的关键毒力蛋白。
- 它对鸡巨噬细胞系 HD11 具有白细胞毒性作用,并能裂解红细胞(RBCs)。
- 该毒素有两个结构域:C端和N端。C端类似于巴斯德菌科的重复毒素(RTX),N端具有溶血和杀白细胞作用。
- 机制:GtxA 与宿主免疫细胞中的肌动蛋白结合,改变细胞形状,阻碍细胞信号传输,从而帮助细菌逃避宿主免疫系统。GtxA 还通过诱导细胞凋亡导致免疫抑制。
2. 菌毛 (Fimbriae):- 属于 F17 样家族(GalF-A),由4个基因编码: flfD, flfC, flfG, flfA 。
- 菌毛蛋白 ( flfA ) 在体内对毒力至关重要,控制组织嗜性。
- G. anatis 通过短菌毛样结构在体外粘附于鸡上皮细胞。
3. 血凝素 (Haemagglutinin):- 血凝素蛋白在生物膜和外膜囊泡(OMVs)中被检测到。
4. 外膜囊泡 (Outer Membrane Vesicles, OMVs):- 促进细菌粘附、定植、生物膜形成以及去除抗生素化合物。
5. 荚膜 (Capsule):- 在细菌与宿主表面的粘附、相互作用及免疫逃避中起重要作用。
- 荚膜敲除突变体(ΔgexD)比野生型毒力更强(这一发现较为独特,通常荚膜缺失会降低毒力,原文如此记录)。
6. 生物膜形成 (Biofilm Formation):- 生物膜对于感染的慢性化、持续时间以及降低对抗生素的敏感性至关重要。
7. 金属蛋白酶 (Metalloproteases):- 用于蛋白水解、增加毒力、定植、营养获取及降解免疫球蛋白 G (IgG)。
8. 延伸因子 Tu (Elongation factor Tu):- 通过囊泡形成释放,具有淀粉样蛋白特性,参与发病机制。
9. 成簇规律间隔短回文重复序列 (CRISPR):- 细菌的先天防御系统,可阻碍转化,表明不同菌株具有不同水平的先天能力。
10. 整合接合元件 (Integrative conjugative elements):
11. 小菌落变异体 (Small colony variants):- 具有溶血活性,有助于细菌存活、复发感染及抗生素耐药性的发展。
12. 其他毒力基因:- cps16A, 16B, 16F (编码糖基转移酶等)。
- fnrG 基因(大肠杆菌 fur 全局调节基因的同源物)。
08致病性 (Pathogenicity)
虽然 G. anatis 是正常微生物组的一部分,但在自然和实验感染中均被证实为关键病原体。- 机会致病与诱发因素: 毒力、感染途径、宿主的免疫状态和年龄都会影响致病性。
- 混合感染: 与病毒(如传染性支气管炎病毒 IBV、低致病性禽流感 H9N2)或细菌(如副鸡禽杆菌 A. paragallinarum 、大肠杆菌 E. coli 、鸡毒支原体 M. gallisepticum )的混合感染会显著增加发病率和死亡率。
- 环境应激: 营养不良、激素紊乱、季节变化(寒冷)、通风不足、过度拥挤和生物安全差均会加重感染。
- 蛋鸡: 导致产蛋量下降(8-10%),死亡率高达73%。引发出血性卵巢炎、卵泡破裂。
- 病理过程: 细菌首先定植于呼吸道(持续4周),然后扩散到生殖器官(卵巢、输卵管、睾丸),导致败血症、卵巢炎、输卵管炎、腹膜炎、肝坏死、心包炎等。
- 毒力差异: 不同地理来源的菌株致病性不同(例如墨西哥分离株致病性略高于中国和奥地利的分离株)。有机鸡群的分离株遗传相似性较高,而种鸡群的分离株遗传多样性更丰富。
09临床表现 (Clinical Manifestations)
G. anatis 感染的临床表现多样且通常非特异性:- 肉鸡: 呼吸道表现,包括鼻分泌物、头部肿胀和震颤、咳嗽、啰音、呼吸困难、腹泻和消瘦。
- 蛋鸡: 产蛋量下降(3-18%),蛋壳质量改变,白色腹泻。
- 混合症状: 许多鸡群表现为混合的呼吸道和生殖道障碍。常见的症状还包括打喷嚏、喘息、头部肿胀。
- 严重病例: 经静脉注射感染的鸡表现为严重的败血症病变、极度抑郁和不愿移动。
- 协同作用: 与副鸡禽杆菌(传染性鼻炎)混合感染时,鼻分泌物和眶下窦肿胀更严重;与大肠杆菌混合感染时,胚胎死亡率更高。
10尸体剖检病变 (Post-mortem Lesions)
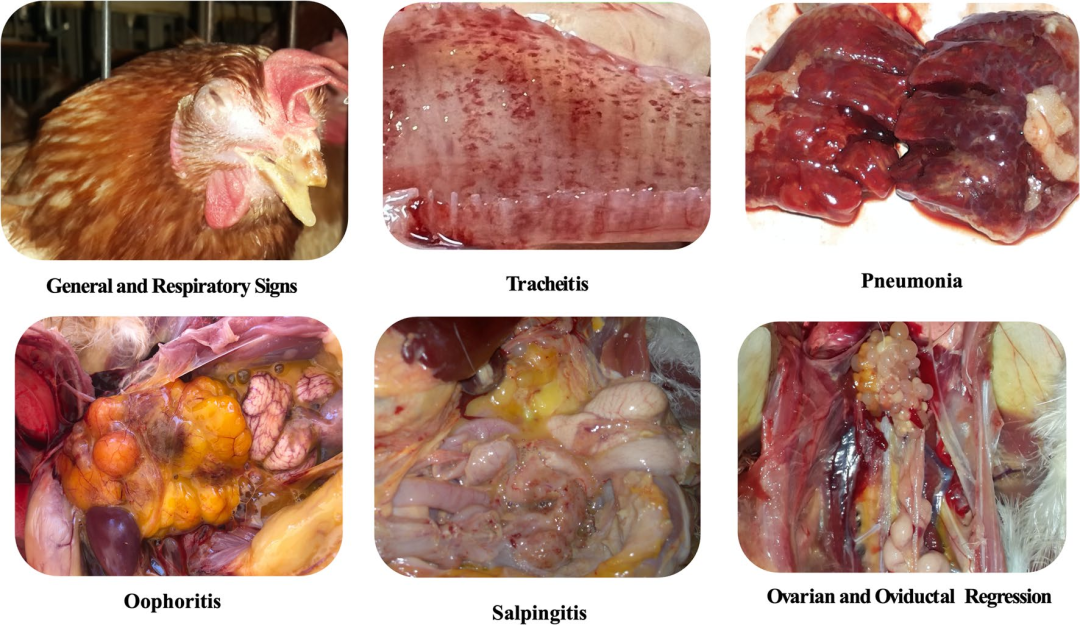
图 2: G. anatis 感染的特征性体征和病变 (Characteristic signs and lesions of G. anatis infection)- 气管炎 (Tracheitis): 从卡他性到化脓性不等。
- 卵巢炎 (Oophoritis): 出血性或化脓性卵巢炎,卵泡变形、破裂、退化。
- 输卵管炎 (Salpingitis): 局灶性或弥漫性,输卵管出血或功能障碍,输卵管内有蛋畸形。
- 卵巢和输卵管退化 (Ovarian and Oviductal Regression)。
- 腹膜炎 (Peritonitis): 纤维素性或化脓性腹膜炎,腹腔内有渗出物。
- 肝周炎 (Perihepatitis): 纤维素性。
- 肝坏死 (Hepatic necrosis): 多灶性。
11诊断 (Diagnosis)
由于临床症状缺乏特异性,必须依靠特定的诊断工具。
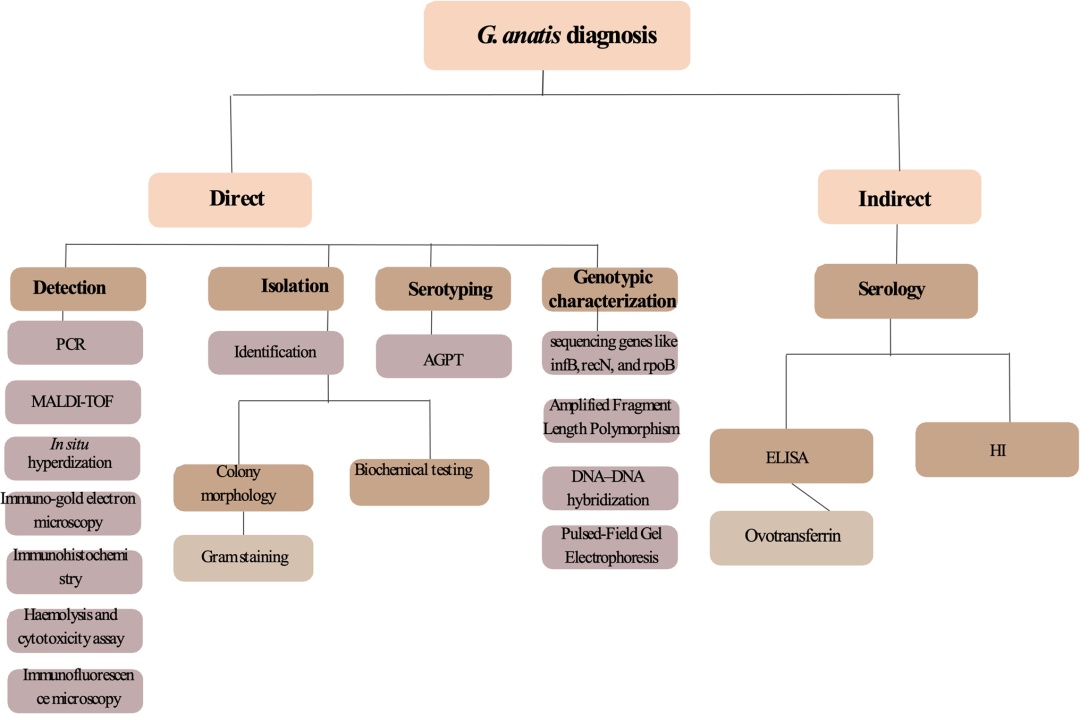
图 3: G. anatis 的不同诊断工具 (Different diagnostic tools of G. anatis )诊断方法主要分为直接法和间接法:
11.1 直接诊断 (Direct)- MALDI-TOF(基质辅助激光解吸/电离飞行时间质谱)。
- 原位杂交 (In situ hybridization)。
- 免疫金电子显微镜 (Immuno-gold electron microscopy)。
- 免疫组织化学 (Immunohistochemistry)。
- 溶血和细胞毒性试验 (Haemolysis and cytotoxicity assay)。
- 免疫荧光显微镜 (Immunofluorescence microscopy)。
- 菌落形态 (Colony morphology)。
- 生化测试 (Biochemical testing)。
- 基因型特征描述 (Genotypic characterization):
- 测序基因(如 infB, recN, rpoB )。
11.2 间接诊断 (Indirect)- ELISA(酶联免疫吸附试验):可检测卵转铁蛋白(Ovotransferrin)作为急性期蛋白标志物。
11.3 分离和表型鉴定 (Isolation and phenotypic identification)- 培养条件: 37°C,24-48小时,含5-10%柠檬酸牛血的血琼脂培养基,微需氧环境。
- 菌落特征: 大多数分离株产生宽的β-溶血带,菌落呈奶油状、圆形、光滑、灰色、无色素且有光泽。
表 2:鉴定 G. anatis 生物型的表型和生化反应 (Phenotypic and biochemical reactions for the identification of G. anatis biotypes)[td]| 特征 | G. anatis biovar haemolytica | G. anatis biovar anatis | G. melopsittaci | G. trehalosifermentans | G. salpingitidis | G. genomospecies 1 | G. genomospecies 2 | G. genomospecies 3 | Gallibacterium group V | | 革兰氏染色 | - | - | - | - | - | - | - | - | - | | 运动性 | - | - | - | - | - | - | - | - | - | | β-溶血 | + | - | - | - | - | - | - | - | - | | 麦康凯生长 | -/D | - | +W | - | + | - | - | D | + | | 过氧化氢酶 | + | + | D | D | + | D | D | D | + | | 氧化酶 | + | + | D | D | + | D | D | D | + | | ONPG | + | + | + | - | + | + | + | + | + | | PNPG | + | + | - | + | - | - | - | - | - | | 磷酸酶 | + | + | + | + | + | + | + | + | + | | 硝酸盐还原 | + | + | + | + | + | + | + | + | + | | 吲哚 | - | - | - | - | - | - | - | D | - | | 脲酶 | - | - | - | - | D | - | - | D | + | | V-P 试验 | - | - | - | - | - | - | - | - | - | | 甲基红 | - | - | - | - | - | D | - | - | - | | H2S | - | - | - | - | - | - | - | - | - | | 柠檬酸盐 | - | - | - | - | - | - | - | - | - | | 蔗糖 | + | + | + | + | + | + | + | + | + | | 麦芽糖 | + | D | + | + | + | + | + | + | + | | 鸟氨酸脱羧酶 | - | + | - | - | - | - | - | - | - | | D-阿拉伯糖 | + | - | D | D | (+) | + | D | D | (+) | | L-阿拉伯糖 | - | - | D | - | + | - | - | D | - | | D-阿拉伯糖醇 | - | - | - | - | + | + | + | D | + | | 木糖醇 | - | - | - | - | +W | - | - | - | - | | 甘油 | + | + | (+) | D | (+) | + | + | D | (+) | | 黏酸盐 | - | - | D | - | + | - | - | D | + | | 乳糖 | - | D | +/(+) | - | (+) | - | - | D | + | | D-葡萄糖 | + | + | + | + | + | + | + | + | + | | D-核糖 | + | + | +/(+) | +/(+) | + | + | + | D | + | | D-山梨醇 | D | D | D | + | D | - | - | D | + | | 海藻糖 | D | + | - | + | - | + | D | - | - | | 棉子糖 | + | + | + | + | +/(+) | + | + | D | + | | 果糖 | + | - | + | + | + | + | + | + | + | | L-岩藻糖 | + | - | D | +/(+) | + | +/(+) | D | D | + | | D-蜜二糖 | - | - | +/(+) | +/(+) | D | - | - | - | + | | D-甘露醇 | + | + | + | + | + | D | D | D | D | | D-甘露糖 | + | + | + | + | + | + | + | + | + | | D-木糖 | + | + | D | + | + | + | + | +/(+) | - | | m-肌醇 | D | D | - | - | - | - | D | - | - | | 糊精 | D | - | - | - | - | (+) | + | - | - | | 半乳糖醇 | - | - | D | D | + | + | + | D | - |
(符号说明:+:所有菌株1-2天内阳性;(+):所有菌株14天内阳性;-:14天后仍阴性;W:弱阳性;D:部分阳性部分阴性)
11.4 分子检测 (Molecular Detection)- PCR: 针对 16S-23S rRNA 内部转录间隔区序列的引物是 Gallibacterium 特异性的。引物 1133fgal 对 Gallibacterium 具有特异性。特定的扩增子大小约为 789, 985 和 1032 bp。
- qPCR(实时定量PCR): 靶向 gyrB 基因或 sodA 基因。比常规 PCR 更快速、敏感、特异且更具成本效益。
- LAMP(环介导等温扩增): 靶向 sodA 基因,比 qPCR 更快更便宜。
11.5 质谱技术 (MALDI-TOF-MS)一种快速、可同时处理大量样本且样本量需求小的技术,可用于确认鸡群间的 G. anatis 克隆谱系。
11.6 其他技术- 血清学: 间接 ELISA 可检测抗体水平(感染后2个月达到峰值)。卵转铁蛋白(Ovotransferrin)可用作急性期蛋白标志物。
- 血凝试验: 利用 G. anatis 对禽类和哺乳动物红细胞的凝集能力。
- 组织病理学: 肝脏可见嗜碱性聚集物(细菌微菌落)被坏死肝细胞包围。脾脏可见多核巨细胞形成。
12预防和控制策略 (Prevention and Control Strategies)
- 生物安全: 实施“全进全出”制度,防止水平传播和耐药基因转移。
- 管理: 控制免疫抑制因子,改善应激条件(如拥挤、通风不良)。
12.1 抗生素治疗 (Antibiotic Treatment)
虽然可以使用抗菌药物,但由于抗原多样性和多重耐药性(MDR)的普遍存在,治疗往往失败。- 埃及 (Elbestawy, 2014; Elewa, 2021): 对土霉素、大观霉素、卡那霉素、新霉素、青霉素、氨苄青霉素表现出极高耐药性(>90%)。
- 摩洛哥 (Nassik et al., 2019): 对氨苄青霉素、红霉素、土霉素和磺胺甲恶唑-甲氧苄啶完全耐药。
- 丹麦/墨西哥 (Bojesen et al., 2011b; Chavez et al., 2017b): 对磺胺甲恶唑和四环素耐药率极高(>90%)。
- 罗马尼亚 (Sorescu et al., 2021): 对四环素类、氟喹诺酮类、氨苄青霉素、甲氧苄啶、萘啶酸和克林霉素耐药。
- 伊朗 (Allahghadry et al., 2021): 低敏感性,建议非抗生素治疗。
- 埃及 (2013-2015): 氟苯尼考、环丙沙星、诺氟沙星、头孢噻肟较敏感。
- 墨西哥: 73%对头孢噻呋敏感,68%对氟苯尼考敏感。
- 尼日利亚: 对头孢噻肟、环丙沙星、多西环素和氟苯尼考高度敏感。
由于MDR的全球性出现(如 tetB, tetH, tetL 基因引起的四环素耐药),使用传统抗生素治疗受到很大限制。替代方案如沸石(zeolites)饲料添加剂、特异性卵黄抗体(IgY) 和 益生菌(如 Leuconostoc mesenteroides )正在研究中。
12.2 疫苗 (Vaccines)- 常规疫苗(灭活菌苗): 墨西哥勃林格殷格翰开发的三价菌苗(含3种生物型,覆盖95%流行株)能提高抗体滴度和产蛋率。自体菌苗也能有效减少临床症状和产蛋下降。
- 亚单位/重组疫苗: 针对 GtxA(特别是N端)、外膜囊泡(OMVs)、菌毛蛋白(FlfA) 的疫苗能提供部分或显著的保护力,减少病变严重程度并提高IgY滴度。
- 多表位疫苗: 针对 GtxA, Gab1309, Gab2348 等免疫原性蛋白的计算机模拟预测显示其具有刺激免疫反应的潜力。
13结论 (Conclusion)
G. anatis 感染正在全球范围内出现并对家禽业造成重大经济损失。其致病性受多种毒力因子(如GtxA、菌毛、荚膜等)、宿主因素及环境应激共同影响。目前,多重耐药性的广泛存在使得传统的抗生素治疗面临巨大挑战。未来的研究应重点关注该病原体的流行病学监测、耐药谱分析以及基于保守抗原(如GtxA)的新型广谱疫苗的开发。
来源:菌中无戏言,作者:凤凰于飞
|
|